21/01/2022
W dziedzinie HVAC (ogrzewanie, wentylacja i klimatyzacja), zrozumienie właściwości gazów jest fundamentalne. Często spotykamy się z terminem "gaz doskonały". Ale co to właściwie znaczy, że gaz jest doskonały? I jakie to ma implikacje dla systemów, z którymi pracujemy? W tym artykule przyjrzymy się bliżej koncepcji gazu doskonałego, jego charakterystycznym cechom, ciepłu właściwemu i różnicom w porównaniu z gazami rzeczywistymi.

Czym jest Gaz Doskonały?
Gaz doskonały, znany również jako gaz idealny, to teoretyczny model gazu, który upraszcza zachowanie gazów rzeczywistych. Jest to koncepcja, która zakłada pewne idealizacje, aby ułatwić obliczenia i zrozumienie termodynamiki gazów. Kluczowe założenia modelu gazu doskonałego to:
- Brak objętości własnej cząsteczek gazu: Zakłada się, że cząsteczki gazu doskonałego są punktowe, co oznacza, że ich objętość jest pomijalnie mała w porównaniu z objętością naczynia, w którym się znajdują. W praktyce, objętość cząsteczek gazów rzeczywistych jest niewielka, ale nie zerowa.
- Brak sił międzycząsteczkowych: W gazie doskonałym zakłada się, że pomiędzy cząsteczkami gazu nie występują żadne siły przyciągania ani odpychania. W rzeczywistości, gazy rzeczywiste wykazują słabe siły międzycząsteczkowe, zwłaszcza w niższych temperaturach i wyższych ciśnieniach.
- Zderzenia sprężyste: Zderzenia między cząsteczkami gazu doskonałego oraz z ściankami naczynia są idealnie sprężyste. Oznacza to, że podczas zderzeń nie traci się energii kinetycznej.
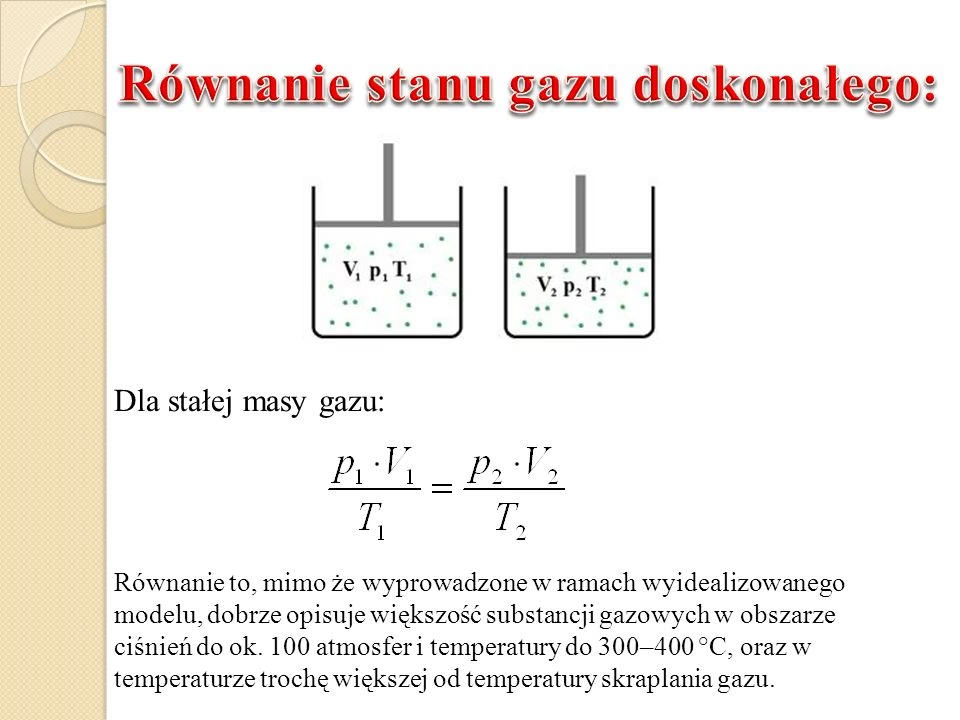
Te założenia prowadzą do prostego równania stanu gazu doskonałego, które jest kluczowe w termodynamice:
pV = nRT
Gdzie:
- p - ciśnienie gazu
- V - objętość gazu
- n - liczba moli gazu
- R - uniwersalna stała gazowa (8,314 J/(mol·K))
- T - temperatura gazu (w Kelwinach)
Równanie to opisuje relację między ciśnieniem, objętością, temperaturą i ilością gazu doskonałego. Jest to potężne narzędzie w analizie procesów termodynamicznych, w tym tych zachodzących w systemach HVAC.
Ciepło Właściwe Gazu Doskonałego
Ciepło właściwe to ilość ciepła potrzebna do podniesienia temperatury jednostki masy substancji o jeden stopień. W przypadku gazów, ciepło właściwe może być definiowane na dwa sposoby: ciepło właściwe przy stałej objętości (CV) i ciepło właściwe przy stałym ciśnieniu (CP).
Dla gazu doskonałego, ciepło właściwe przy stałej objętości (CV) jest związane ze zmianą energii wewnętrznej (ΔU). Przy stałej objętości, całe dostarczone ciepło idzie na zwiększenie energii wewnętrznej gazu, ponieważ praca objętościowa (praca wykonana przez gaz na otoczenie) jest równa zeru (ponieważ objętość się nie zmienia).
Matematycznie, możemy to zapisać jako:
qV = ΔU = nCVΔT
Gdzie:
- qV - ciepło dostarczone przy stałej objętości
- ΔU - zmiana energii wewnętrznej
- n - liczba moli gazu
- CV - molowe ciepło właściwe przy stałej objętości
- ΔT - zmiana temperatury
Dla gazu doskonałego monoatomowego (np. hel, neon, argon), molowe ciepło właściwe przy stałej objętości (CV) wynosi:
CV = (3/2)R ≈ 12,47 J/(mol·K)
Wartość ta wynika z faktu, że energia wewnętrzna gazu monoatomowego jest związana tylko z energią kinetyczną ruchu postępowego cząsteczek (trzy stopnie swobody).

Dla gazów dwuatomowych i wieloatomowych, CV jest wyższe, ponieważ energia wewnętrzna obejmuje również energię rotacyjną i wibracyjną cząsteczek. Jednak dla gazów doskonałych nadal możemy stosować uproszczone modele, zwłaszcza w umiarkowanych temperaturach.
Co się Dzieje z Gazem Doskonałym, Gdy Dodamy Ciepło?
Reakcja gazu doskonałego na dodanie ciepła zależy od warunków, w jakich proces zachodzi. Rozważmy dwa kluczowe przypadki:
Dodawanie Ciepła przy Stałej Objętości
Jak wspomniano wcześniej, przy stałej objętości (proces izochoryczny), całe dostarczone ciepło idzie na zwiększenie energii wewnętrznej gazu. Ponieważ objętość jest stała, gaz nie wykonuje pracy na otoczenie (W = 0). W rezultacie, temperatura gazu wzrasta proporcjonalnie do dostarczonego ciepła i ciepła właściwego przy stałej objętości (CV).
W tym przypadku, cała energia cieplna jest przekształcana w energię kinetyczną cząsteczek gazu, co objawia się wzrostem temperatury.
Dodawanie Ciepła przy Stałym Ciśnieniu
Przy stałym ciśnieniu (proces izobaryczny), sytuacja jest nieco inna. Gdy dostarczamy ciepło do gazu doskonałego przy stałym ciśnieniu, część tego ciepła idzie na zwiększenie energii wewnętrznej (a tym samym temperatury), a część na wykonanie pracy objętościowej, czyli rozprężanie gazu przeciwko stałemu ciśnieniu zewnętrznemu.

W tym przypadku, do osiągnięcia tej samej zmiany temperatury, potrzebujemy dostarczyć więcej ciepła niż przy stałej objętości. Definiujemy ciepło właściwe przy stałym ciśnieniu (CP), które jest większe niż CV dla gazu doskonałego.
Relacja między CP i CV dla gazu doskonałego jest prosta i wyraża się wzorem:
CP = CV + R
Gdzie R to uniwersalna stała gazowa. To równanie odzwierciedla fakt, że przy stałym ciśnieniu, dodatkowe ciepło jest potrzebne na wykonanie pracy objętościowej.
Gaz Doskonały a Gaz Rzeczywisty: Różnice
Gaz doskonały jest modelem uproszczonym, który dobrze opisuje zachowanie gazów rzeczywistych w pewnych warunkach, zwłaszcza przy niskich ciśnieniach i wysokich temperaturach. W tych warunkach, cząsteczki gazu są od siebie na tyle odległe, że ich objętość własna staje się pomijalna, a siły międzycząsteczkowe stają się słabe.

Jednak w warunkach wysokich ciśnień i niskich temperatur, założenia modelu gazu doskonałego przestają być dokładne. Gazy rzeczywiste:
- Posiadają objętość własną cząsteczek: Przy wysokich ciśnieniach, objętość cząsteczek gazu staje się znacząca w porównaniu z całkowitą objętością, co wpływa na zachowanie gazu.
- Wykazują siły międzycząsteczkowe: Przy niskich temperaturach, energia kinetyczna cząsteczek jest mniejsza, a siły przyciągania międzycząsteczkowe stają się bardziej istotne. Siły te mogą wpływać na ciśnienie gazu i prowadzić do odchyleń od równania stanu gazu doskonałego.
Aby dokładniej opisywać gazy rzeczywiste, stosuje się bardziej zaawansowane równania stanu, takie jak równanie Van der Waalsa, które uwzględniają objętość własną cząsteczek i siły międzycząsteczkowe. Równanie Van der Waalsa wprowadza dwa parametry korekcyjne (a i b) do równania stanu gazu doskonałego, aby uwzględnić te efekty.
Mimo tych różnic, koncepcja gazu doskonałego jest niezwykle użyteczna w wielu zastosowaniach inżynierskich, w tym w HVAC. W większości warunków pracy systemów HVAC, powietrze i inne gazy robocze można z dobrym przybliżeniem traktować jako gazy doskonałe. Uproszczenie to znacznie ułatwia analizę i projektowanie systemów.
Znaczenie Gazów Doskonałych w HVAC
Zrozumienie gazów doskonałych jest kluczowe w projektowaniu i analizie systemów HVAC z kilku powodów:
- Obliczenia termodynamiczne: Równanie stanu gazu doskonałego i koncepcje ciepła właściwego są fundamentem obliczeń termodynamicznych, które są niezbędne do projektowania i analizy cykli chłodniczych, systemów grzewczych i wentylacyjnych.
- Analiza procesów: Zrozumienie, jak gazy doskonałe reagują na dodawanie ciepła przy stałej objętości i stałym ciśnieniu, pomaga w analizie różnych procesów termodynamicznych zachodzących w systemach HVAC, takich jak sprężanie, rozprężanie, ogrzewanie i chłodzenie.
- Projektowanie systemów: Wiedza o właściwościach gazów doskonałych umożliwia inżynierom projektowanie bardziej efektywnych i energooszczędnych systemów HVAC, poprzez optymalizację procesów i dobór odpowiednich komponentów.
- Diagnostyka i rozwiązywanie problemów: Zrozumienie odchyleń od zachowania gazu doskonałego może pomóc w diagnozowaniu problemów w systemach HVAC i identyfikacji przyczyn nieprawidłowego działania.
Często Zadawane Pytania (FAQ)
- Czy powietrze jest gazem doskonałym?
W większości zastosowań HVAC, powietrze można traktować jako gaz doskonały z dobrym przybliżeniem. W normalnych temperaturach i ciśnieniach roboczych, odchylenia od zachowania gazu doskonałego są niewielkie. Jednak w ekstremalnych warunkach (bardzo niskie temperatury lub bardzo wysokie ciśnienia), model gazu rzeczywistego byłby bardziej odpowiedni. - Jakie gazy w systemach HVAC można uważać za doskonałe?
Wiele gazów roboczych stosowanych w systemach HVAC, takich jak czynniki chłodnicze (np. R-134a, R-410A) i gazy nośne (np. azot), można w praktyce traktować jako gazy doskonałe w zakresie typowych warunków pracy. - Kiedy model gazu doskonałego przestaje być dokładny w HVAC?
Model gazu doskonałego może stać się mniej dokładny w systemach HVAC pracujących przy bardzo niskich temperaturach (np. w kriogenicznych systemach chłodniczych) lub bardzo wysokich ciśnieniach (np. w sprężarkach wysokociśnieniowych). W takich przypadkach, konieczne może być uwzględnienie efektów gazów rzeczywistych. - Czy ciepło właściwe gazu doskonałego jest stałe?
Ciepło właściwe gazu doskonałego zależy od temperatury, ale w pewnym zakresie temperatur można je uważać za w miarę stałe, zwłaszcza w typowych zakresach temperatur pracy systemów HVAC. Jednak dla dokładniejszych obliczeń, należy uwzględnić zależność ciepła właściwego od temperatury.
Podsumowanie
Koncepcja gazu doskonałego jest niezwykle ważna w dziedzinie HVAC. Pozwala na uproszczenie analizy i projektowania systemów grzewczych, wentylacyjnych i klimatyzacyjnych. Chociaż gazy rzeczywiste różnią się od idealnego modelu, w większości zastosowań HVAC, założenia gazu doskonałego są wystarczająco dokładne do praktycznych celów. Zrozumienie właściwości gazów doskonałych, ich ciepła właściwego i reakcji na dodawanie ciepła, jest kluczowe dla inżynierów i techników pracujących w branży HVAC, umożliwiając im projektowanie i utrzymywanie efektywnych i niezawodnych systemów.
Jeśli chcesz poznać inne artykuły podobne do Gazy Doskonałe: Właściwości i Zastosowania w HVAC, możesz odwiedzić kategorię HVAC.
