02/02/2020
W świecie termodynamiki, procesy izobaryczne odgrywają kluczową rolę w zrozumieniu zachowania gazów, a w szczególności gazów doskonałych. Ogrzewanie izobaryczne, jak sama nazwa wskazuje, to proces termodynamiczny zachodzący przy stałym ciśnieniu. Jest to fundamentalne pojęcie, które znajduje zastosowanie w wielu dziedzinach, od inżynierii mechanicznej po meteorologię. Zrozumienie tego procesu jest niezbędne dla każdego, kto zajmuje się systemami HVAC (ogrzewanie, wentylacja i klimatyzacja) oraz szeroko pojętą inżynierią cieplną.
https://www.youtube.com/watch?v=0gcJCfcAhR29_xXO
Czym dokładnie jest proces izobaryczny?
Jak już wspomniano, proces izobaryczny charakteryzuje się stałością ciśnienia. Wyobraźmy sobie cylinder z ruchomym tłokiem, w którym znajduje się gaz doskonały. Jeśli dostarczymy ciepło do gazu, ale jednocześnie pozwolimy tłokowi na swobodne przemieszczanie się tak, aby ciśnienie wewnątrz cylindra pozostało stałe, to właśnie mamy do czynienia z procesem izobarycznym. W praktyce oznacza to, że objętość gazu i jego temperatura mogą się zmieniać, ale ciśnienie pozostaje niezmienne.

Matematyczny opis procesu izobarycznego
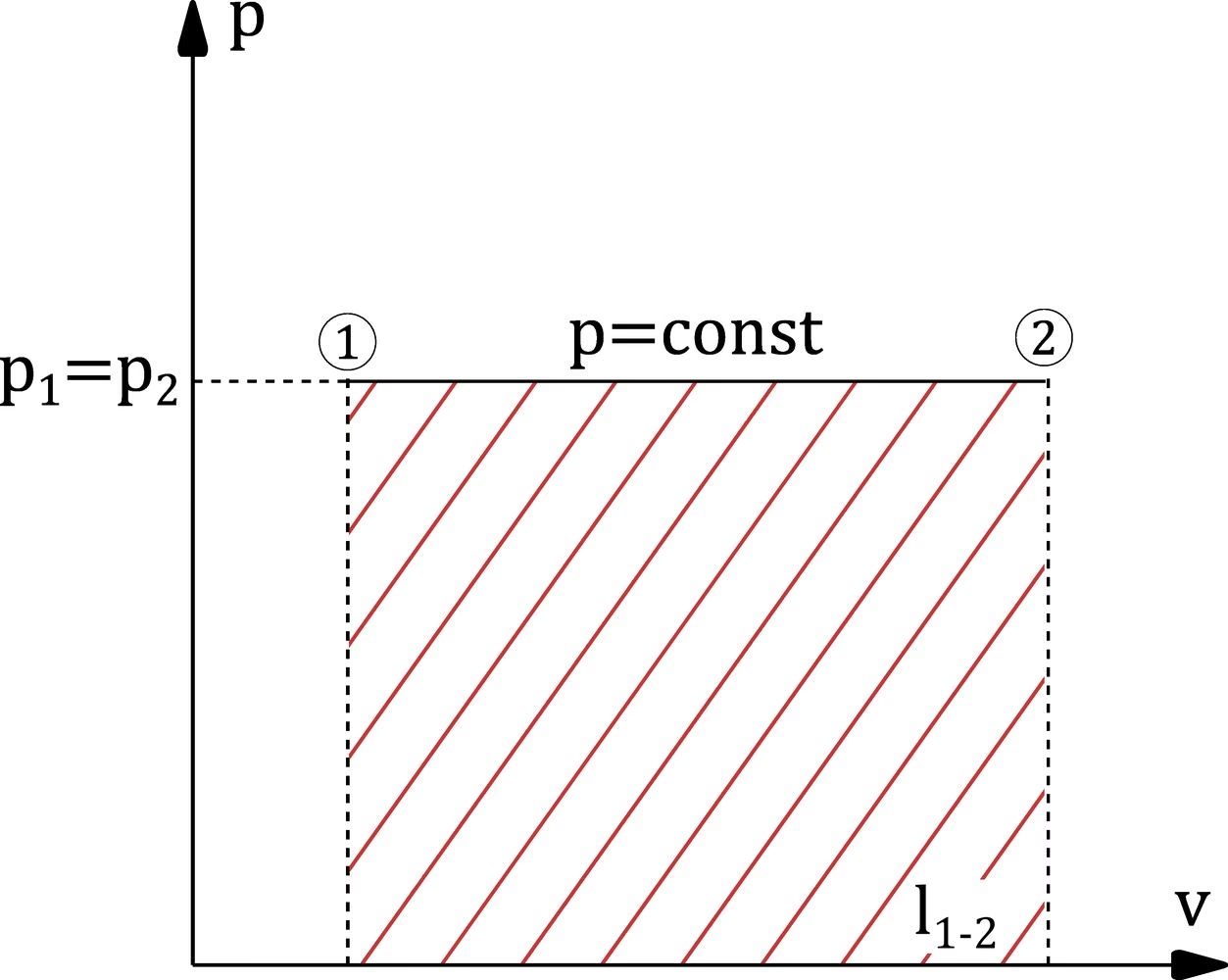
Aby lepiej zrozumieć proces izobaryczny, warto przyjrzeć się jego opisowi matematycznemu. Podstawowe równanie opisujące pracę wykonaną przez gaz w procesie izobarycznym jest stosunkowo proste:
W = P(V2 - V1)
Gdzie:
- W - praca wykonana przez gaz
- P - stałe ciśnienie
- V1 - objętość początkowa gazu
- V2 - objętość końcowa gazu
To równanie pokazuje, że praca wykonana przez gaz w procesie izobarycznym jest wprost proporcjonalna do zmiany objętości i stałego ciśnienia. Jeśli objętość gazu wzrasta (V2 > V1), praca jest dodatnia, co oznacza, że gaz wykonuje pracę nad otoczeniem. Jeśli objętość gazu maleje (V2 < V1), praca jest ujemna, co oznacza, że otoczenie wykonuje pracę nad gazem.
Związek z prawem Gay-Lussaca
Dla gazów doskonałych, proces izobaryczny jest ściśle związany z prawem Gay-Lussaca, znanym również jako prawo Charlesa i Gay-Lussaca. Prawo to mówi, że przy stałym ciśnieniu, objętość gazu doskonałego jest wprost proporcjonalna do jego temperatury bezwzględnej:
V/T = const.
Lub inaczej:
V1/T1 = V2/T2
Z tego prawa wynika, że jeśli w procesie izobarycznym dostarczamy ciepło do gazu, co powoduje wzrost jego temperatury, to jednocześnie musi wzrosnąć jego objętość, aby ciśnienie pozostało stałe. Odwrotnie, jeśli gaz jest chłodzony przy stałym ciśnieniu, jego objętość musi się zmniejszyć.
Ogrzewanie izobaryczne a inne izoprocesy
Proces izobaryczny jest jednym z czterech podstawowych izoprocesów gazu doskonałego. Pozostałe trzy to:
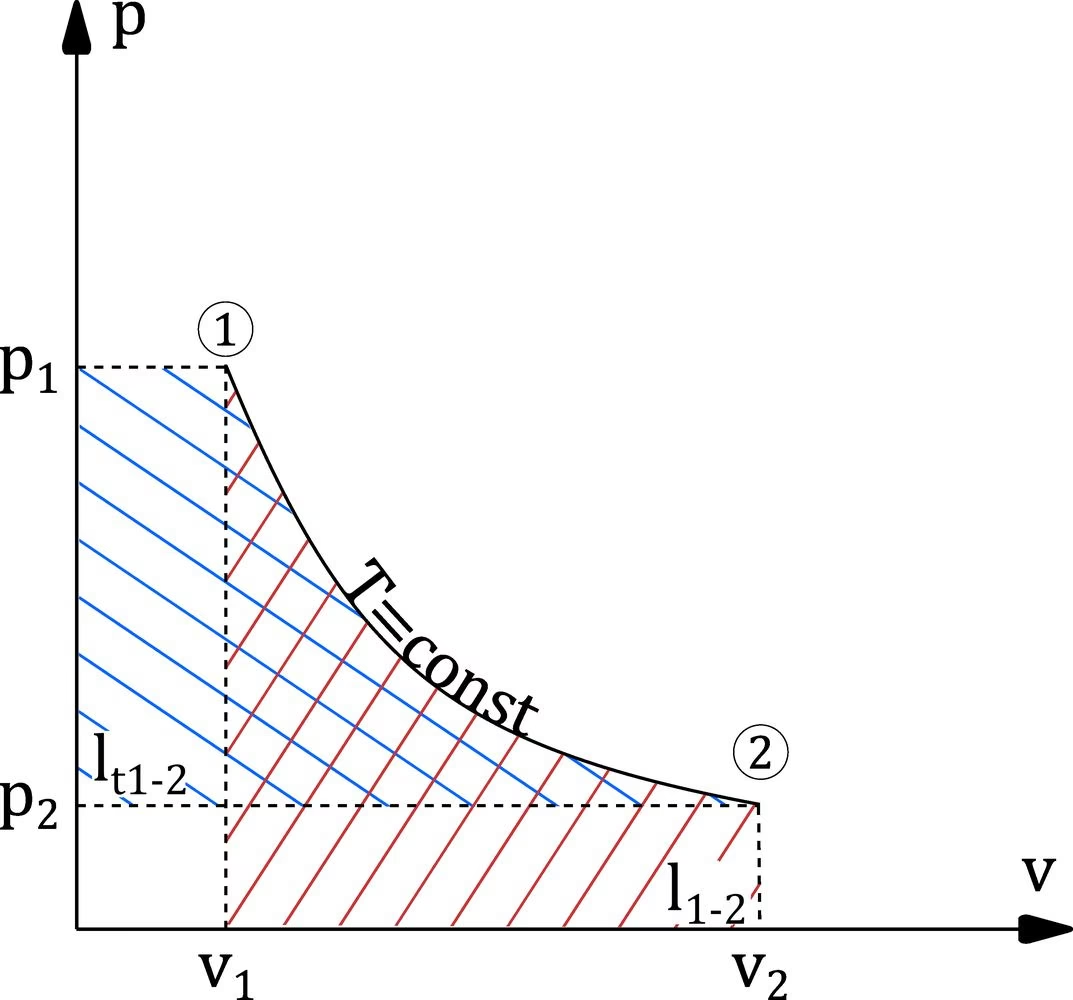
- Proces izotermiczny: zachodzi przy stałej temperaturze (T = const.).
- Proces izochoryczny: zachodzi przy stałej objętości (V = const.).
- Proces adiabatyczny: zachodzi bez wymiany ciepła z otoczeniem (Q = 0).
Poniższa tabela przedstawia porównanie tych procesów, uwzględniając ich definicje, prawa, równania stanu i pierwszą zasadę termodynamiki:
| Proces | Definicja | Prawo | Równanie stanu | I zasada termodynamiki | Uwagi |
|---|---|---|---|---|---|
| Izotermiczny | T = const. | Boyle’a-Mariotte’a | pV = const. | ΔU = 0; |ΔQ| = |ΔW|; ΔW = nRTln(V2/V1) | Rurka Meldego |
| Izobaryczny | p = const. | Gay-Lussaca | V/T = const. | ΔW = pΔV = nRΔT; ΔQ = nCPΔT = mCPΔT; ΔU = nCVΔT | |
| Izochoryczny | V = const. | Charlesa | p/T = const. | ΔW = 0; ΔU = ΔQ = nCVΔT; ΔU = nCVΔT | Termometr gazowy |
| Adiabatyczny | ΔQ = 0 | Poissona | pVκ = const. | ΔU = ΔW; ΔW = nCVΔT = CVΔ(pV)/R |
Z tabeli jasno widać, że każdy izoproces ma swoje unikalne cechy i implikacje dotyczące pracy, ciepła i energii wewnętrznej gazu. W kontekście ogrzewania izobarycznego, kluczowe jest zrozumienie, że dostarczone ciepło jest wykorzystywane zarówno do zwiększenia energii wewnętrznej gazu (co objawia się wzrostem temperatury), jak i do wykonania pracy poprzez zwiększenie objętości gazu.

Pierwsza zasada termodynamiki w procesie izobarycznym
Pierwsza zasada termodynamiki, która jest zasadą zachowania energii, ma fundamentalne znaczenie w analizie procesów termodynamicznych, w tym procesu izobarycznego. Zasada ta stwierdza, że zmiana energii wewnętrznej układu (ΔU) jest równa sumie dostarczonego ciepła (ΔQ) i pracy wykonanej nad układem (ΔW) lub przez układ (-ΔW):
ΔU = ΔQ - ΔW
Dla procesu izobarycznego, możemy wyrazić poszczególne składniki tej zasady:
- Zmiana energii wewnętrznej (ΔU): ΔU = nCVΔT, gdzie n to liczba moli gazu, CV to molowe ciepło właściwe przy stałej objętości, a ΔT to zmiana temperatury.
- Ciepło (ΔQ): ΔQ = nCPΔT, gdzie CP to molowe ciepło właściwe przy stałym ciśnieniu. Zauważmy, że CP jest większe niż CV, ponieważ przy stałym ciśnieniu część dostarczonego ciepła jest wykorzystywana na wykonanie pracy, a nie tylko na zwiększenie energii wewnętrznej.
- Praca (ΔW): ΔW = pΔV = nRΔT, jak wspomniano wcześniej.
Podstawiając te wyrażenia do pierwszej zasady termodynamiki, możemy zauważyć, że wszystko się zgadza i energia jest zachowana.
Zastosowania ogrzewania izobarycznego
Proces ogrzewania izobarycznego znajduje szerokie zastosowanie w różnych dziedzinach. Kilka przykładów:
- Systemy HVAC: W systemach ogrzewania, wentylacji i klimatyzacji, procesy izobaryczne są wykorzystywane w wymiennikach ciepła, gdzie powietrze lub czynnik chłodniczy jest ogrzewany lub chłodzony przy stałym ciśnieniu.
- Silniki spalinowe: W silnikach spalinowych, faza rozprężania po zapłonie paliwa może być w przybliżeniu modelowana jako proces izobaryczny, choć w rzeczywistości jest to bardziej złożony proces.
- Procesy przemysłowe: W wielu procesach przemysłowych, takich jak destylacja, suszenie czy ogrzewanie w kotłach, procesy izobaryczne odgrywają istotną rolę.
- Meteorologia: Procesy izobaryczne są ważne w meteorologii, na przykład przy analizie rozszerzania się ogrzanego powietrza w atmosferze przy stałym ciśnieniu atmosferycznym.
Pytania i odpowiedzi (FAQ)
Czy w procesie ogrzewania izobarycznego temperatura zawsze wzrasta?
Tak, w procesie ogrzewania izobarycznego gazu doskonałego, temperatura zawsze wzrasta, jeśli dostarczamy ciepło do układu. Zgodnie z prawem Gay-Lussaca, przy stałym ciśnieniu, wzrost objętości gazu jest wprost proporcjonalny do wzrostu temperatury. Dostarczanie ciepła powoduje wzrost energii wewnętrznej gazu, co manifestuje się wzrostem temperatury i objętości, przy zachowaniu stałego ciśnienia.
Co się dzieje z energią wewnętrzną gazu podczas ogrzewania izobarycznego?
Energia wewnętrzna gazu wzrasta podczas ogrzewania izobarycznego. Dostarczone ciepło jest wykorzystywane zarówno na zwiększenie energii wewnętrznej gazu, jak i na wykonanie pracy poprzez rozszerzanie się gazu przeciwko stałemu ciśnieniu zewnętrznemu. Zmiana energii wewnętrznej jest proporcjonalna do zmiany temperatury i ciepła właściwego przy stałej objętości (ΔU = nCVΔT).
Jak obliczyć ciepło dostarczone w procesie ogrzewania izobarycznego?
Ciepło dostarczone w procesie ogrzewania izobarycznego można obliczyć za pomocą wzoru: ΔQ = nCPΔT, gdzie n to liczba moli gazu, CP to molowe ciepło właściwe przy stałym ciśnieniu, a ΔT to zmiana temperatury. Wartość CP zależy od rodzaju gazu i jest zazwyczaj większa niż ciepło właściwe przy stałej objętości (CV).
Czy proces sprężania izobarycznego jest możliwy?
Tak, proces sprężania izobarycznego jest możliwy. W takim przypadku, praca jest wykonywana nad gazem, a ciepło jest odprowadzane z gazu, aby utrzymać stałe ciśnienie. Podczas sprężania izobarycznego, temperatura gazu maleje, a jego objętość się zmniejsza. Zgodnie z pierwszą zasadą termodynamiki, zmiana energii wewnętrznej jest równa sumie dostarczonej pracy (dodatniej) i odprowadzonego ciepła (ujemnego).
Podsumowanie
Ogrzewanie izobaryczne gazu doskonałego jest ważnym procesem termodynamicznym, który charakteryzuje się stałym ciśnieniem. Zrozumienie tego procesu jest kluczowe dla inżynierów i techników pracujących w branży HVAC i termodynamiki. Proces ten jest opisany prawem Gay-Lussaca i pierwszą zasadą termodynamiki, a jego znajomość pozwala na analizę i projektowanie systemów, w których zachodzą przemiany termodynamiczne przy stałym ciśnieniu. Mam nadzieję, że ten artykuł pomógł w zrozumieniu istoty ogrzewania izobarycznego i jego znaczenia w świecie nauki i technologii.
Jeśli chcesz poznać inne artykuły podobne do Ogrzewanie Izobaryczne Gazu Doskonałego: Kompletny Przewodnik, możesz odwiedzić kategorię HVAC.