27/08/2017
Wodorotlenki żelaza, a w szczególności wodorotlenek żelaza(II) (Fe(OH)2) i wodorotlenek żelaza(III) (Fe(OH)3), to nieorganiczne związki chemiczne o istotnym znaczeniu w chemii i przemyśle. Choć oba zawierają żelazo i grupy hydroksylowe, różnią się właściwościami, sposobami otrzymywania i zastosowaniami. Niniejszy artykuł ma na celu szczegółowe omówienie tych dwóch wodorotlenków, ich charakterystykę oraz porównanie kluczowych aspektów.

Jak powstaje wodorotlenek żelaza(II) - Fe(OH)2?
Wodorotlenek żelaza(II) można łatwo otrzymać w laboratorium poprzez reakcję strąceniową. Najpopularniejszą metodą jest reakcja roztworu soli żelaza(II), takiej jak chlorek żelaza(II) (FeCl2) lub siarczan(VI) żelaza(II) (FeSO4), z roztworem silnej zasady, na przykład wodorotlenku potasu (KOH) lub wodorotlenku sodu (NaOH). Reakcja ta prowadzi do wytrącenia osadu wodorotlenku żelaza(II) z roztworu. Przykładowa reakcja z siarczanem(VI) żelaza(II) i wodorotlenkiem potasu wygląda następująco:
FeSO4 + 2KOH → Fe(OH)2 ↓ + K2SO4
Strzałka w dół (↓) przy Fe(OH)2 symbolizuje wytrącanie się osadu z roztworu.
Oczyszczanie wodorotlenku żelaza(II)
Aby uzyskać bardziej czysty produkt, surowy osad wodorotlenku żelaza(II) można poddać procesowi oczyszczania. Jedną z metod jest rozpuszczenie osadu w stężonym roztworze amoniaku (NH3aq). Następnie, roztwór ten rozcieńcza się dużą ilością wody, co powoduje ponowne wytrącenie wodorotlenku żelaza(II). Proces ten wykorzystuje różnice w rozpuszczalności wodorotlenku żelaza(II) w różnych środowiskach. Dodatkowo, mieszaninę można ogrzewać do temperatury około 80°C, co sprzyja wzrostowi ziaren osadu i przyspiesza proces precypitacji. Ostatnim etapem oczyszczania jest suszenie osadu. Stosuje się liofilizację (suszenie sublimacyjne), a następnie umieszcza się osuszony produkt w wysokiej próżni w obecności pięciotlenku fosforu (P2O5), który działa jako silny środek suszący, usuwając resztki wody.
Charakter chemiczny wodorotlenku żelaza(II)
Wodorotlenek żelaza(II) wykazuje charakter amfoteryczny. Oznacza to, że może reagować zarówno z kwasami, jak i z zasadami. W przeciwieństwie do niektórych innych wodorotlenków metali, Fe(OH)2 nie reaguje z wodą.
Reakcje z kwasami
W reakcji z kwasami, wodorotlenek żelaza(II) zachowuje się jak zasada, neutralizując kwas i tworząc sól i wodę. Przykładowo, reakcja z kwasem chlorowodorowym (HCl) przebiega następująco:
Fe(OH)2 + 2HCl → FeCl2 + 2H2O
W formie jonowej, reakcję można zapisać jako:
Fe(OH)2 + 2H+ + 2Cl- → Fe2+ + 2Cl- + 2H2O
Jak widać, wodorotlenek żelaza(II) reaguje z jonami wodorowymi (H+) z kwasu, tworząc jony żelaza(II) (Fe2+) i wodę.

Reakcje z zasadami
Amfoteryczny charakter Fe(OH)2 ujawnia się również w reakcjach z mocnymi zasadami. W tych reakcjach, wodorotlenek żelaza(II) zachowuje się jak kwas, reagując z zasadą i tworząc kompleksowy związek. Reakcja z wodorotlenkiem potasu (KOH) prowadzi do powstania tetrahydroksyżelazianu(II) potasu, związku kompleksowego:
Fe(OH)2 + 2KOH → K2[Fe(OH)4]
Wodorotlenek żelaza(III) - Fe(OH)3
Wodorotlenek żelaza(III) (Fe(OH)3) to nieorganiczny związek chemiczny o odmiennych właściwościach w porównaniu do Fe(OH)2. Jest to ciało stałe o charakterystycznej czerwono-brunatnej barwie. Należy jednak zaznaczyć, że „czysty” wodorotlenek żelaza(III) w ścisłym tego słowa znaczeniu nie został wyizolowany. W rzeczywistości, to co określamy jako wodorotlenek żelaza(III) ma zmienny skład i jest lepiej opisywane wzorem ogólnym xFe2O3·yH2O, co wskazuje na hydratowaną formę tlenku żelaza(III).
Nierozpuszczalność i tlenowodorotlenki żelaza(III)
Wodorotlenek żelaza(III) jest praktycznie nierozpuszczalny w wodzie i alkoholu. Częściowo odwodniona forma o wzorze Fe(O)OH, znana jako tlenowodorotlenek żelaza(III), występuje naturalnie jako minerały, takie jak goethyt i lepidokrokit. Te minerały są ważnymi składnikami rud żelaza.
Otrzymywanie wodorotlenku żelaza(III)
Roztwory koloidalne wodorotlenku żelaza(III) można otrzymać poprzez dodanie mocnej zasady, na przykład wodorotlenku sodu (NaOH), do roztworu soli żelaza(III), takiej jak chlorek żelaza(III) (FeCl3). Reakcja ta prowadzi do wytrącenia brunatnego, galaretowatego osadu:
FeCl3 + 3NaOH → Fe(OH)3 ↓ + 3NaCl
Aby uzyskać koloid wolny od obcych jonów, można zastosować hydrolizę etanolanu żelaza(III) (Fe(OC2H5)3). Hydroliza, czyli reakcja z wodą, prowadzi do powstania koloidalnego roztworu wodorotlenku żelaza(III).
Zastosowania wodorotlenku żelaza(III)
Pomimo swojej nierozpuszczalności, wodorotlenek żelaza(III) znajduje zastosowanie w praktyce. Jest wykorzystywany jako pigment, nadając charakterystyczną czerwoną barwę farbom i pigmentom. Ponadto, ze względu na swoje właściwości adsorpcyjne, jest stosowany w procesach oczyszczania wody, pomagając w usuwaniu zanieczyszczeń.
Porównanie wodorotlenku żelaza(II) i wodorotlenku żelaza(III)
Poniższa tabela przedstawia porównanie kluczowych właściwości i charakterystyk wodorotlenku żelaza(II) i wodorotlenku żelaza(III):
| Właściwość | Wodorotlenek żelaza(II) - Fe(OH)2 | Wodorotlenek żelaza(III) - Fe(OH)3 |
|---|---|---|
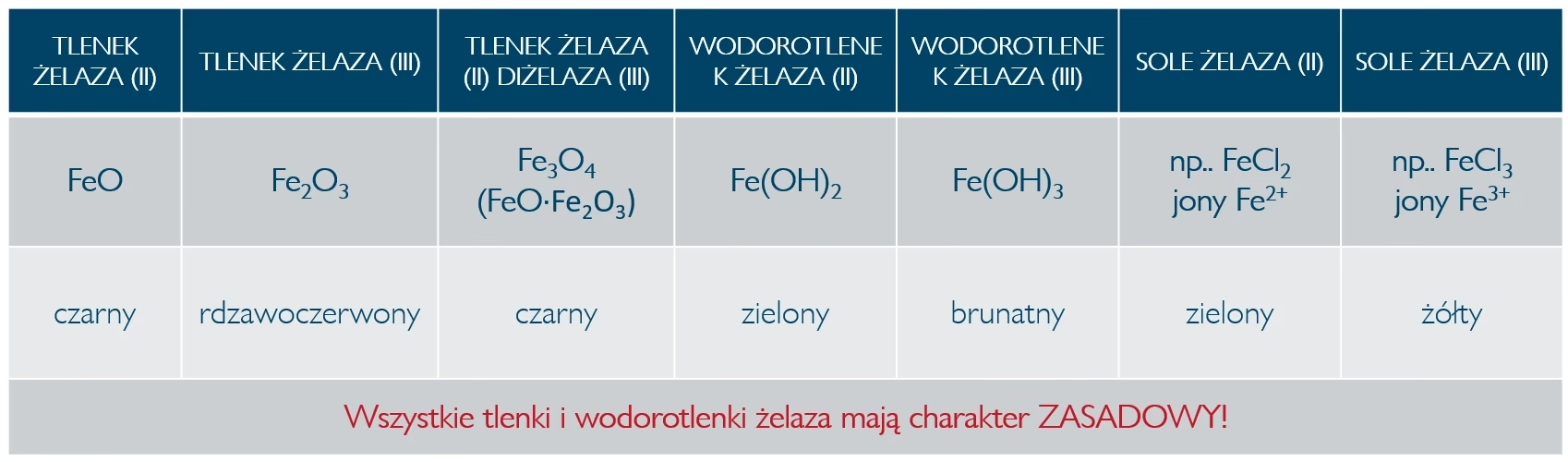
| Barwa | Biało-zielonkawy (szybko ciemnieje na powietrzu) | Czerwono-brunatny |
| Rozpuszczalność w wodzie | Praktycznie nierozpuszczalny | Praktycznie nierozpuszczalny |
| Charakter chemiczny | Amfoteryczny | Zasadniczy (słabo amfoteryczny) |
| Reakcja z kwasami | Reaguje, tworząc sole żelaza(II) | Reaguje, tworząc sole żelaza(III) |
| Reakcja z zasadami | Reaguje, tworząc związki kompleksowe | Słaba lub brak reakcji |
| Sposób otrzymywania | Reakcja soli żelaza(II) z zasadami | Reakcja soli żelaza(III) z zasadami, hydroliza etanolanu żelaza(III) |
| Skład | Fe(OH)2 | xFe2O3·yH2O (hydratowany tlenek żelaza(III)) |
Najczęściej zadawane pytania (FAQ)
Czym różni się wodorotlenek żelaza(II) od wodorotlenku żelaza(III)?
Główna różnica polega na stopniu utlenienia żelaza. W wodorotlenku żelaza(II) żelazo występuje na stopniu utlenienia +2 (Fe2+), natomiast w wodorotlenku żelaza(III) na stopniu utlenienia +3 (Fe3+). Powoduje to różnice w barwie, charakterze chemicznym i reaktywności.
Czy wodorotlenek żelaza(II) jest szkodliwy?
Wodorotlenek żelaza(II) nie jest uważany za substancję silnie toksyczną, jednak należy unikać jego spożycia i kontaktu ze skórą oraz oczami. Pył wodorotlenku żelaza(II) może działać drażniąco na drogi oddechowe.
Jak przechowywać wodorotlenek żelaza(II)?
Wodorotlenek żelaza(II) jest wrażliwy na działanie tlenu z powietrza i łatwo ulega utlenieniu do wodorotlenku żelaza(III). Dlatego należy przechowywać go w szczelnie zamkniętych pojemnikach, w atmosferze beztlenowej lub w obecności substancji redukujących, aby zapobiec utlenieniu.
Gdzie można znaleźć wodorotlenek żelaza(III) w naturze?
Wodorotlenek żelaza(III), a dokładniej tlenowodorotlenek żelaza(III) w formie minerałów goethytu i lepidokrocytu, jest szeroko rozpowszechniony w przyrodzie i stanowi ważny składnik rud żelaza, gleb i osadów.
Podsumowanie
Wodorotlenek żelaza(II) i wodorotlenek żelaza(III) to interesujące i ważne związki chemiczne. Choć oba są wodorotlenkami żelaza, wykazują istotne różnice w swoich właściwościach i zastosowaniach. Wodorotlenek żelaza(II) o charakterze amfoterycznym i wodorotlenek żelaza(III) stosowany jako pigment i w oczyszczaniu wody, stanowią przykłady wszechstronności chemii żelaza i jego związków nieorganicznych.
Jeśli chcesz poznać inne artykuły podobne do Wodorotlenek żelaza(II) i żelaza(III): Porównanie i Właściwości, możesz odwiedzić kategorię HVAC.