13/05/2022
Kwas węglowy, choć może brzmi tajemniczo, jest substancją, z którą mamy do czynienia na co dzień, a w kontekście systemów HVAC (ogrzewanie, wentylacja i klimatyzacja) odgrywa on istotną, choć często niedocenianą rolę. Powstaje w wyniku prostej reakcji chemicznej, która zachodzi, gdy dwutlenek węgla (CO2) rozpuszcza się w wodzie (H2O). Ta pozornie nieskomplikowana reakcja ma szerokie implikacje, wpływając na pH wody, procesy korozyjne i równowagę chemiczną w systemach chłodzenia i grzewczych.

Reakcja syntezy: CO2 + H2O → H2CO3
Reakcja tworzenia kwasu węglowego jest klasyfikowana jako reakcja syntezy. W chemii reakcja syntezy ma miejsce, gdy dwa lub więcej substratów łączy się, tworząc jeden produkt. W tym konkretnym przypadku, dwutlenek węgla (CO2) i woda (H2O) łączą się, tworząc kwas węglowy (H2CO3). Równanie reakcji jest proste i eleganckie, ale kryje w sobie złożone procesy termodynamiczne i kinetyczne:
CO2 + H2O → H2CO3
Choć reakcja wydaje się prosta, warto zanurzyć się głębiej w jej naturę i zrozumieć, dlaczego kwas węglowy jest tak specyficzny i dlaczego jego zachowanie różni się od innych kwasów.
Związek między CO2 a kwasem węglowym w naturze
Naturalnie, kwas węglowy powstaje, gdy dwutlenek węgla obecny w atmosferze rozpuszcza się w wodach oceanów i innych zbiornikach wodnych. Oceany absorbują znaczną część dwutlenku węgla emitowanego do atmosfery, szacuje się, że około 30%. Wraz ze wzrostem poziomu atmosferycznego CO2, spowodowanego działalnością człowieka, taką jak spalanie paliw kopalnych i zmiany w użytkowaniu gruntów, ilość dwutlenku węgla absorbowanego przez oceany również wzrasta.
Gdy CO2 jest absorbowany przez wodę morską, zachodzi szereg reakcji chemicznych, które prowadzą do wzrostu stężenia jonów wodorowych (H+). Ten proces ma dalekosiężne konsekwencje dla oceanów i żyjących w nich organizmów, prowadząc do zjawiska zakwaszenia oceanów. Skala pH, która mierzy kwasowość i zasadowość substancji, jest kluczowa w zrozumieniu tego procesu. Skala pH rozciąga się od 0 do 14, gdzie 7 oznacza pH neutralne. Wartości powyżej 7 wskazują na odczyn zasadowy (alkaliczny), a wartości poniżej 7 na odczyn kwasowy. Skala pH jest odwrotnością stężenia jonów wodorowych – im więcej jonów wodorowych, tym wyższa kwasowość i niższe pH.
Woda i dwutlenek węgla łączą się, tworząc kwas węglowy (H2CO3), słaby kwas, który dysocjuje na jony wodorowe (H+) i jony wodorowęglanowe (HCO3-). To właśnie obecność jonów wodorowych obniża pH wody.
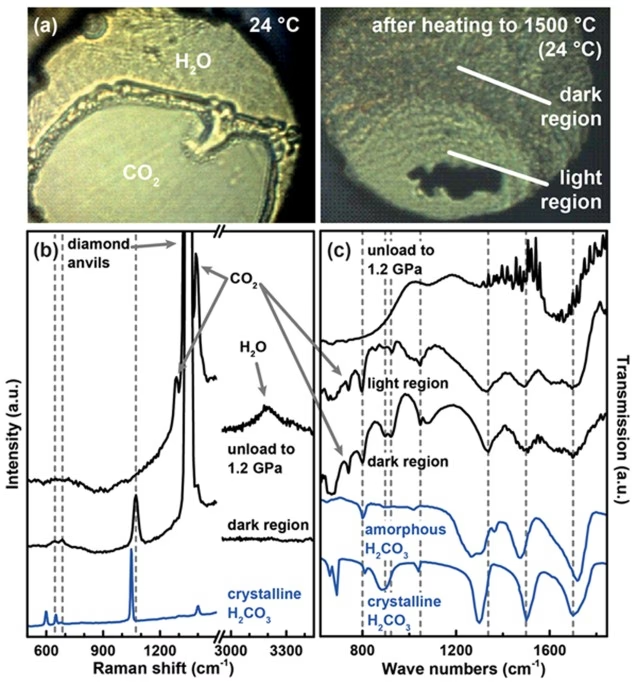
Endotermiczna natura reakcji CO2 + H2O → H2CO3
Reakcja tworzenia kwasu węglowego jest reakcją endotermiczną, co oznacza, że wymaga dostarczenia energii w postaci ciepła, aby mogła zajść. Entalpia tej reakcji wynosi +2.2 kJ, co potwierdza jej endotermiczny charakter. Co więcej, reakcja ta nie jest spontaniczna w standardowych warunkach temperatury i ciśnienia (STP) ze względu na ograniczenia termodynamiczne, co ilustruje skuteczność drugiej zasady termodynamiki.
Przemiana gazu (CO2) w ciecz (H2CO3 w roztworze wodnym) generuje ujemną entropię (-340.49 J/K), co również wpływa na spontaniczność reakcji. W rezultacie, energia swobodna Gibbsa reakcji w temperaturze 298.15 K (25°C) wynosi +103.67 kJ, co wskazuje na brak spontaniczności w tych warunkach. Dodatnia wartość energii swobodnej Gibbsa potwierdza, że reakcja jest odwracalna i preferuje kierunek przeciwny do tworzenia kwasu węglowego.
dG = dH – T ds = 2.2 - 298.15 * (- 0.34049) = +103.67 kJ
Powyższe wyliczenia jasno pokazują, że reakcja tworzenia kwasu węglowego, nawet w temperaturze pokojowej, nie jest spontaniczna i jest bardziej skłonna do przebiegania w kierunku odwrotnym.
Kinetka reakcji i stabilność kwasu węglowego
Oprócz termodynamiki, kluczowa jest również kinetyka reakcji. Ustalanie się równowagi między rozpuszczonym CO2 a kwasem węglowym (CO2 (aq) + H2O (l) ⇌ H2CO3 (aq)) jest procesem kinetycznie powolnym. Jest to reakcja samopodtrzymująca się – w miarę rozkładu niestabilnego kwasu węglowego, równowaga jest utrzymywana poprzez rozpuszczanie większej ilości CO2. Proces ten trwa nieustannie, dopóki dostępne są CO2 i woda.

W warunkach braku katalizatora, równowaga osiągana jest bardzo powoli. W stanie równowagi, tylko niewielka frakcja (około 0.2-1%) rozpuszczonego CO2 jest rzeczywiście przekształcana w H2CO3. Większość CO2 pozostaje w postaci solwatowanych cząsteczek CO2. Stała równowagi (K) tej reakcji w temperaturze 298.15 K wynosi zaledwie 1.7 x 10^-3, co potwierdza, że większość dwutlenku węgla nie jest przekształcana w kwas węglowy i pozostaje jako cząsteczki CO2.
K = [H2CO3] / [CO2] = 1.7 X 10^-3
Stałe szybkości reakcji również potwierdzają te obserwacje. Szybkość reakcji w kierunku tworzenia kwasu węglowego (CO2 + H2O → H2CO3) wynosi 0.039 s−1, natomiast szybkość reakcji odwrotnej (H2CO3 → CO2 + H2O) jest znacznie większa i wynosi 23 s−1. To ponownie podkreśla, że reakcja w temperaturze 298.15 K nie jest spontaniczna, a reakcja odwrotna przebiega znacznie szybciej.
Rola anhydrazy węglanowej
W organizmach żywych, reakcja CO2 + H2O → H2CO3 jest znacznie przyspieszana dzięki obecności enzymu anhydrazy węglanowej. Anhydraza węglanowa jest metaloenzymem, który katalizuje wzajemne przemiany między CO2 i H2O oraz kwasem węglowym (H2CO3) i jego jonami dysocjacyjnymi (HCO3− i H+). Enzym ten reguluje pH i wspomaga transport CO2 w organizmach. W kontekście systemów HVAC, choć anhydraza węglanowa nie jest bezpośrednio wykorzystywana, zrozumienie jej działania podkreśla, jak ważna jest kinetyka reakcji i jak katalizatory mogą wpływać na procesy chemiczne związane z kwasem węglowym.
Dlaczego kwas węglowy nie zastąpi kwasu siarkowego w wieżach chłodniczych?
Często pojawia się pytanie, czy CO2 można by wykorzystać jako zamiennik kwasu siarkowego (H2SO4) w wieżach chłodniczych do regulacji pH wody. W praktyce, choć próby takie były podejmowane, kwas węglowy ma istotne ograniczenia w tym zastosowaniu.
Wprowadzenie CO2 do wody chłodzącej tymczasowo przesuwa równowagę węglanową w kierunku wodorowęglanów, ponieważ powstawanie kwasu węglowego obniża pH. Może to działać w systemach z wodą obiegową o niższym pH. Jednak uwolniony CO2 jest usuwany w wieży chłodniczej. W rezultacie, pH wody chłodzącej powraca do stanu równowagi, gdy woda przepływa przez wypełnienie wieży chłodniczej, a CO2 jest uwalniany do atmosfery. Usuwanie CO2 z wody chłodzącej ogranicza jego użyteczność do kontroli pH w otwartych systemach. Alkaliczność M wody w wieży pozostaje zasadniczo niezmieniona.
Kwas siarkowy, jako mocny kwas, trwale obniża pH i nie ulega tak łatwemu usuwaniu z wody w otwartym systemie, co czyni go bardziej efektywnym w długoterminowej kontroli pH w wieżach chłodniczych. Kwas węglowy, ze względu na swoją niestabilność i tendencję do rozkładu do CO2 i H2O, nie jest praktycznym zamiennikiem kwasu siarkowego w tego typu aplikacjach.
Podsumowanie
Kwas węglowy, choć słaby i niestabilny, jest wszechobecny i odgrywa istotną rolę w systemach HVAC. Jego powstawanie w wyniku reakcji CO2 z wodą wpływa na pH wody, co ma znaczenie dla procesów korozyjnych i równowagi chemicznej. Zrozumienie termodynamiki i kinetyki reakcji tworzenia kwasu węglowego pozwala lepiej zarządzać systemami wodnymi w instalacjach HVAC i optymalizować ich działanie. Pomimo swoich ograniczeń, wiedza o kwasie węglowym jest kluczowa dla efektywnego i bezpiecznego projektowania i eksploatacji systemów ogrzewania, wentylacji i klimatyzacji.
Jeśli chcesz poznać inne artykuły podobne do Kwas węglowy: Niewidzialny aktor w systemach HVAC, możesz odwiedzić kategorię HVAC.
