23/03/2026
Czy zastanawiałeś się kiedyś, jak z wody – prostej substancji – można uzyskać wodór i tlen? Elektroliza wody to fascynujący proces, który umożliwia rozkład wody na jej podstawowe składniki za pomocą energii elektrycznej. Jest to kluczowa technologia w kontekście produkcji czystego wodoru i zrównoważonej energii. W tym artykule zgłębimy tajniki elektrolizy wody, zrozumiemy jej chemiczne podstawy, zastosowania i odpowiemy na najczęściej zadawane pytania.
- Czym jest elektroliza wody?
- Chemia elektrolizy wody – reakcje i podstawy
- Wpływ temperatury na elektrolizę
- Efektywność elektrolizy – dlaczego nie jest 100%?
- Kolory w elektrolizie wody – co oznaczają?
- Co się wytrąca podczas elektrolizy wody?
- Elektroliza wodoru – produkcja zielonego wodoru
- Elektrolizery – rodzaje i zasada działania
- Zastosowania elektrolizy i elektrolizerów
- Rodzaje elektrolizy – nie tylko woda
- Podsumowanie – elektroliza kluczem do przyszłości?
- Często zadawane pytania (FAQ)
Czym jest elektroliza wody?
Elektroliza wody to proces elektrochemiczny, w którym woda (H2O) jest rozkładana na wodór (H2) i tlen (O2) pod wpływem prądu elektrycznego. Proces ten zachodzi w elektrolizerze, urządzeniu, które umożliwia kontrolowane przeprowadzenie elektrolizy. Aby elektroliza była efektywna, woda zazwyczaj musi zawierać elektrolit, substancję zwiększającą przewodnictwo elektryczne, na przykład wodorotlenek sodu (NaOH) lub kwas siarkowy (H2SO4). Bez elektrolitu czysta woda przewodzi prąd elektryczny bardzo słabo, co znacznie spowalnia proces elektrolizy.
Chemia elektrolizy wody – reakcje i podstawy
Podczas elektrolizy wody zachodzą reakcje redoks – redukcja i utlenianie. Na katodzie (elektrodzie ujemnej) dochodzi do redukcji jonów wodorowych (H+), które w środowisku wodnym pochodzą z dysocjacji wody. Reakcja katodowa wygląda następująco:
2H+ + 2e- → H2
Powstający wodór gazowy wydziela się na katodzie.
Na anodzie (elektrodzie dodatniej) zachodzi utlenianie jonów wodorotlenkowych (OH-) lub, w przypadku elektrolizy roztworów kwaśnych, bezpośrednio wody. Reakcja anodowa (w środowisku obojętnym lub zasadowym) jest następująca:
4OH- → O2 + 2H2O + 4e-
Lub, w środowisku kwaśnym:
2H2O → O2 + 4H+ + 4e-
W wyniku reakcji anodowej powstaje tlen gazowy, który wydziela się na anodzie. Sumaryczna reakcja elektrolizy wody to:
2H2O → 2H2 + O2
Warto zauważyć, że objętość wodoru gazowego powstałego podczas elektrolizy jest dwukrotnie większa niż objętość tlenu, co wynika ze stechiometrii reakcji.

Wpływ temperatury na elektrolizę
Temperatura ma istotny wpływ na efektywność elektrolizy. Wyższa temperatura zazwyczaj przyspiesza reakcję elektrolizy. Dzieje się tak z kilku powodów:
- Zwiększenie przewodnictwa elektrolitu: W wyższych temperaturach ruchliwość jonów w roztworze wzrasta, co prowadzi do lepszego przewodnictwa elektrycznego elektrolitu. Dzięki temu prąd elektryczny może łatwiej przepływać przez roztwór, co przyspiesza proces elektrolizy.
- Szybsza kinetyka reakcji: Wyższa temperatura zwiększa energię kinetyczną cząsteczek, co przyspiesza reakcje chemiczne zachodzące na elektrodach. Zarówno reakcja redukcji wodoru na katodzie, jak i utleniania tlenu na anodzie, przebiegają szybciej w wyższej temperaturze.
- Zmniejszenie nadnapięcia:Nadnapięcie to dodatkowa energia potrzebna do pokonania barier aktywacji reakcji elektrodowych. W wyższych temperaturach nadnapięcie zazwyczaj maleje, co oznacza, że elektroliza staje się bardziej efektywna energetycznie.
Jednak zbyt wysoka temperatura może również prowadzić do niepożądanych efektów, takich jak zwiększone parowanie wody lub korozja materiałów elektrodowych. Dlatego optymalna temperatura elektrolizy zależy od konkretnych warunków i użytych materiałów.
Efektywność elektrolizy – dlaczego nie jest 100%?
Efektywność elektrolizy rzadko osiąga 100%. Istnieje kilka czynników, które wpływają na to, że proces nie jest w pełni wydajny:
- Reakcje uboczne: W praktyce, oprócz głównej reakcji elektrolizy wody, mogą zachodzić reakcje uboczne. Na przykład, w roztworach zawierających chlorki, na anodzie może zachodzić utlenianie jonów chlorkowych do chloru gazowego, co obniża wydajność produkcji tlenu.
- Nadnapięcie: Jak wspomniano wcześniej, elektroliza wody wymaga dodatkowej energii w postaci nadnapięcia, aby pokonać bariery aktywacji. Bez nadnapięcia elektroliza zachodzi bardzo powoli lub wcale. Nadnapięcie jest związane z kinetyką reakcji elektrodowych i zależy od materiału elektrod, temperatury i gęstości prądu.
- Straty energii: Część energii elektrycznej dostarczonej do elektrolizera jest tracona na ciepło z powodu oporu elektrycznego roztworu i elektrod. Straty te są nieuniknione i obniżają całkowitą efektywność energetyczną procesu.
- Rekombinacja gazów: W pewnych warunkach wodór i tlen mogą rekombinować z powrotem do wody na powierzchni elektrod, co zmniejsza ilość gazów uzyskanych w wyniku elektrolizy.
Aby zwiększyć efektywność elektrolizy, naukowcy i inżynierowie pracują nad nowymi materiałami elektrodowymi, elektrolitami i konstrukcjami elektrolizerów, które minimalizują straty i reakcje uboczne.
Kolory w elektrolizie wody – co oznaczają?
Obserwacja kolorów podczas elektrolizy wody może dostarczyć cennych informacji o procesie i potencjalnych zanieczyszczeniach. Oto kilka przykładów:
- Bezbarwny: Idealna elektroliza czystej wody destylowanej powinna być bezbarwna. Brak koloru wskazuje na czystość roztworu i brak zanieczyszczeń, które mogłyby wpływać na barwę.
- Zielonkawy: Pojawienie się koloru zielonkawego może sugerować obecność jonów miedzi (Cu2+). Miedź może pochodzić z korozji elektrod miedzianych lub zanieczyszczeń w wodzie. Miedź w roztworze elektrolitu może wpływać na reakcje elektrodowe i efektywność elektrolizy.
- Brunatny:Brunatny kolor może wskazywać na obecność jonów żelaza (Fe2+ lub Fe3+). Żelazo może pochodzić z korozji elektrod stalowych lub zanieczyszczeń. Podobnie jak miedź, żelazo może wpływać na proces elektrolizy i zanieczyszczać produkowane gazy.
- Żółtawy:Żółtawy odcień może sugerować obecność jonów chloru (Cl-) lub innych związków halogenowych. Chlor może powstawać w wyniku elektrolizy roztworów zawierających chlorki lub być obecny jako zanieczyszczenie. Chlor gazowy jest toksyczny i niepożądany w produkcji wodoru lub tlenu.
Warto pamiętać, że intensywność kolorów zależy od stężenia zanieczyszczeń i rodzaju elektrolitu. Obserwacja kolorów jest prostym, ale przydatnym narzędziem do monitorowania procesu elektrolizy.
Co się wytrąca podczas elektrolizy wody?
Podczas elektrolizy wody mogą wytrącać się różne substancje, głównie na powierzchni elektrod. Osady te mogą być wynikiem:
- Korozji elektrod: Elektrody, szczególnie te wykonane z mniej odpornych materiałów, mogą ulegać korozji w środowisku elektrolitycznym. Produkty korozji, takie jak tlenki metali, mogą wytrącać się na elektrodach lub w roztworze.
- Zanieczyszczeń w wodzie: Woda użyta do elektrolizy, nawet woda wodociągowa, może zawierać zanieczyszczenia, takie jak sole mineralne, metale ciężkie, czy substancje organiczne. Niektóre z tych zanieczyszczeń mogą wytrącać się podczas elektrolizy, tworząc osady.
- Reakcji elektrolitu: W niektórych przypadkach sam elektrolit może brać udział w reakcjach ubocznych, prowadząc do powstania trudno rozpuszczalnych produktów, które wytrącają się z roztworu.
Wytrącanie się osadów może zmniejszać efektywność elektrolizy, zatykać elektrody i utrudniać przepływ prądu. Dlatego ważne jest stosowanie czystej wody, odpowiednich materiałów elektrodowych i elektrolitów, które minimalizują ryzyko wytrącania się niepożądanych osadów.
Elektroliza wodoru – produkcja zielonego wodoru
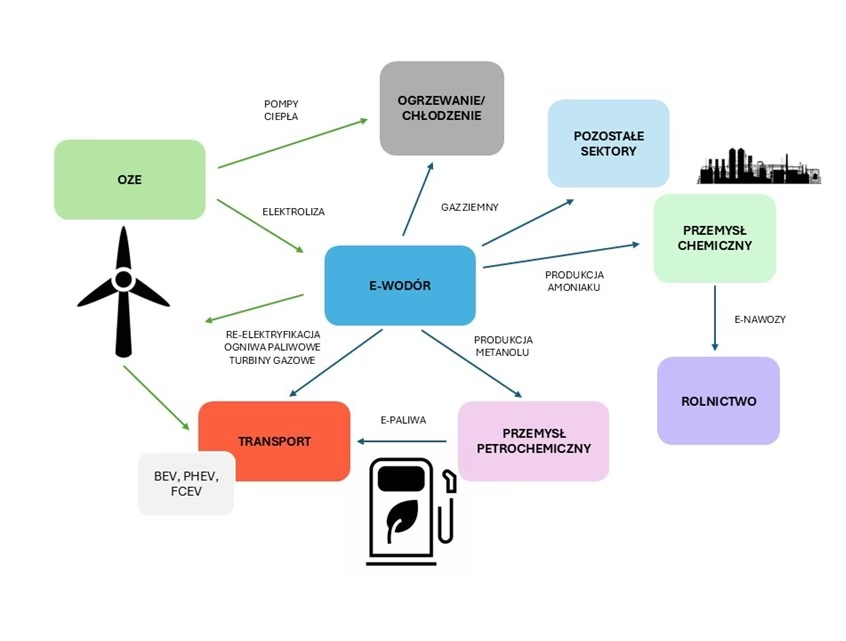
Elektroliza jest kluczową technologią w produkcji zielonego wodoru, który jest uważany za paliwo przyszłości. Zielony wodór to wodór produkowany w sposób zrównoważony, z wykorzystaniem odnawialnych źródeł energii (OZE), takich jak energia słoneczna, wiatrowa czy wodna. Proces produkcji zielonego wodoru poprzez elektrolizę wody jest następujący:
- Pobór energii OZE: Energia elektryczna z paneli słonecznych, turbin wiatrowych lub elektrowni wodnych jest kierowana do elektrolizera.
- Elektroliza wody: W elektrolizerze energia elektryczna jest wykorzystywana do rozkładu wody na wodór i tlen.
- Odzysk i magazynowanie wodoru: Wodór gazowy jest oddzielany od tlenu, oczyszczany i magazynowany.
Produkcja zielonego wodoru poprzez elektrolizę wody z OZE jest bezemisyjna, ponieważ jedynym produktem ubocznym jest tlen. Wodór produkowany w ten sposób może być wykorzystywany jako paliwo w ogniwach paliwowych, w przemyśle chemicznym, transporcie i energetyce, przyczyniając się do redukcji emisji gazów cieplarnianych i walki ze zmianami klimatycznymi.
Elektrolizery – rodzaje i zasada działania
Elektrolizer to urządzenie przeznaczone do przeprowadzania elektrolizy wody. Istnieje kilka rodzajów elektrolizerów, różniących się technologią i zastosowaniem:
- Elektrolizer PEM (Proton Exchange Membrane): Wykorzystuje membranę polimerową przewodzącą protony (H+). Elektrolizery PEM charakteryzują się wysoką efektywnością, kompaktową budową i bezpieczeństwem. Są idealne do zastosowań, gdzie wymagana jest wysoka czystość wodoru i elastyczność pracy.
- Elektrolizer alkaliczny: Jest to najbardziej dojrzała i ekonomiczna technologia. Wykorzystuje roztwór alkaliczny (np. KOH lub NaOH) jako elektrolit. Elektrolizery alkaliczne są stosowane na dużą skalę w przemyśle do produkcji wodoru i tlenu.
- Elektrolizer SOEC (Solid Oxide Electrolysis Cell): Wykorzystuje stały tlenek jako elektrolit i pracuje w wysokich temperaturach (700-900°C). Elektrolizery SOEC charakteryzują się bardzo wysoką efektywnością energetyczną, ale są wciąż w fazie rozwoju i komercjalizacji.
- Przydomowy elektrolizer wodoru: Mniejsze elektrolizery przeznaczone do użytku domowego, często zasilane energią słoneczną lub wiatrową. Pozwalają na produkcję wodoru na własne potrzeby, np. do zasilania małych urządzeń lub magazynowania energii.
Wszystkie elektrolizery działają na podobnej zasadzie: przepuszczają prąd elektryczny przez wodę zawierającą elektrolit, co prowadzi do rozkładu wody na wodór i tlen na elektrodach.

Zastosowania elektrolizy i elektrolizerów
Elektroliza i elektrolizery znajdują szerokie zastosowanie w różnych dziedzinach:
- Przemysł chemiczny: Produkcja chloru, sody kaustycznej, aluminium, wodoru, tlenu i wielu innych substancji chemicznych. Elektroliza jest kluczowym procesem w wielu gałęziach przemysłu.
- Energetyka: Produkcja zielonego wodoru jako paliwa i nośnika energii. Magazynowanie energii odnawialnej w postaci wodoru. Ogniwa paliwowe zasilane wodorem.
- Transport:Pojazdy wodorowe (samochody, autobusy, pociągi, statki) zasilane ogniwami paliwowymi.
- Oczyszczanie wody:Dezynfekcja wody poprzez elektrolityczne generowanie ozonu i innych środków utleniających. Usuwanie zanieczyszczeń z wody.
- Medycyna i kosmetologia:Depilacja elektrolityczna – trwałe usuwanie owłosienia. Produkcja substancji farmaceutycznych.
- Edukacja i badania naukowe: Demonstracje procesów chemicznych, badania nad nowymi materiałami elektrodowymi i elektrolitami, rozwój nowych technologii elektrolizy.
Rodzaje elektrolizy – nie tylko woda
Elektroliza nie ogranicza się tylko do wody. Istnieją różne rodzaje elektrolizy, w zależności od substancji poddawanej elektrolizie i użytego elektrolitu:
- Elektroliza stopionych soli: Rozkład stopionych soli (np. NaCl, Al2O3) na pierwiastki składowe. Stosowana w produkcji metali, takich jak aluminium, sód, magnez.
- Elektroliza roztworów wodnych soli: Np. elektroliza roztworu NaCl prowadzi do produkcji chloru, wodoru i sody kaustycznej.
- Elektroliza kwasów: Np. elektroliza kwasu solnego (HCl) prowadzi do produkcji chloru i wodoru.
- Elektroliza wodorotlenków: Elektroliza roztworów wodorotlenku potasu (KOH) lub sodu (NaOH) jest często stosowana do produkcji wodoru i tlenu na skalę przemysłową.
Podsumowanie – elektroliza kluczem do przyszłości?
Elektroliza to niezwykle ważny proces chemiczny, który odgrywa kluczową rolę w wielu dziedzinach naszego życia. Od produkcji zielonego wodoru, przez przemysł chemiczny, aż po kosmetologię – zastosowania elektrolizy są szerokie i różnorodne. W kontekście globalnych wyzwań klimatycznych i potrzeby transformacji energetycznej, elektroliza wody, szczególnie w połączeniu z odnawialnymi źródłami energii, staje się coraz ważniejsza. Produkcja czystego wodoru poprzez elektrolizę ma potencjał zrewolucjonizować sektor energetyczny i transportowy, przyczyniając się do budowy zrównoważonej przyszłości.
Chociaż elektroliza nie jest procesem idealnym i wciąż istnieją wyzwania związane z jej efektywnością i kosztami, ciągły rozwój technologii, badania nad nowymi materiałami i optymalizacja procesów, sprawiają, że elektroliza staje się coraz bardziej dostępna i opłacalna. Czy elektroliza jest kluczem do przyszłości energetycznej świata? Wszystko wskazuje na to, że tak, a dalszy rozwój tej fascynującej technologii przyniesie jeszcze wiele innowacyjnych rozwiązań.
Często zadawane pytania (FAQ)
- Czy ciepło przyspiesza elektrolizę?
Tak, wyższa temperatura zazwyczaj przyspiesza elektrolizę wody, zwiększając przewodnictwo elektrolitu i szybkość reakcji. - Dlaczego elektroliza nie jest w 100% efektywna?
Efektywność elektrolizy jest ograniczona przez reakcje uboczne, nadnapięcie, straty energii i rekombinację gazów. - Jaka woda powinna być używana do elektrolizy?
Najlepiej używać wody destylowanej lub dejonizowanej z dodatkiem elektrolitu, aby zwiększyć przewodnictwo. - Czy elektroliza wody jest bezpieczna w domu?
Przydomowa elektroliza wymaga zachowania ostrożności ze względu na prąd elektryczny i łatwopalny wodór. Należy przestrzegać zasad bezpieczeństwa i regulacji prawnych. - Jakie są przyszłe perspektywy elektrolizy?
Przyszłość elektrolizy jest obiecująca, zwłaszcza w kontekście produkcji zielonego wodoru i rozwoju zrównoważonej energetyki. Ciągły rozwój technologii i obniżanie kosztów sprawiają, że elektroliza staje się coraz bardziej konkurencyjna.
Autor: Maciej Waliduda, specjalista ds. uzdatniania wody
Jeśli chcesz poznać inne artykuły podobne do Elektroliza Wody: Kompleksowy Przewodnik, możesz odwiedzić kategorię HVAC.
