21/07/2021
Wodorotlenek miedzi(II) jest związkiem chemicznym o wielu interesujących właściwościach i reakcjach. Jedną z nich jest reakcja z glicerolem, alkoholem polihydroksylowym, szeroko stosowanym w różnych gałęziach przemysłu. Czy glicerol reaguje z wodorotlenkiem miedzi? Odpowiedź brzmi: tak, i jest to reakcja bardzo charakterystyczna, wykorzystywana w chemii do identyfikacji tego typu związków.

Reakcja Glicerolu z Wodorotlenkiem Miedzi(II)
Glicerol, znany również jako gliceryna, jest trihydroksyalkoholem, co oznacza, że w swojej strukturze posiada trzy grupy hydroksylowe (-OH). Wodorotlenek miedzi(II), o wzorze chemicznym Cu(OH)2, w środowisku zasadowym reaguje z glicerolem, tworząc kompleksowy związek chemiczny. Charakterystycznym objawem tej reakcji jest zmiana koloru roztworu.
Świeżo strącony wodorotlenek miedzi(II) ma postać niebieskiego, galaretowatego osadu. Jednak po dodaniu glicerolu i utrzymaniu środowiska zasadowego (na przykład poprzez dodanie wodorotlenku sodu NaOH), osad rozpuszcza się, a roztwór przybiera intensywny, ciemnoniebieski kolor. Ten kolor jest wynikiem powstania kompleksu miedzi(II) z glicerolem.
Reakcja ta zachodzi, ponieważ glicerol, jako poliol, zdolny jest do tworzenia kompleksów z jonami metali, w tym z jonami miedzi(II). Grupy hydroksylowe glicerolu koordynują się z jonem miedzi(II), tworząc strukturę kompleksową, która jest rozpuszczalna w wodzie i charakteryzuje się intensywnym niebieskim zabarwieniem.
Zastosowanie Reakcji Glicerolu z Wodorotlenkiem Miedzi(II)
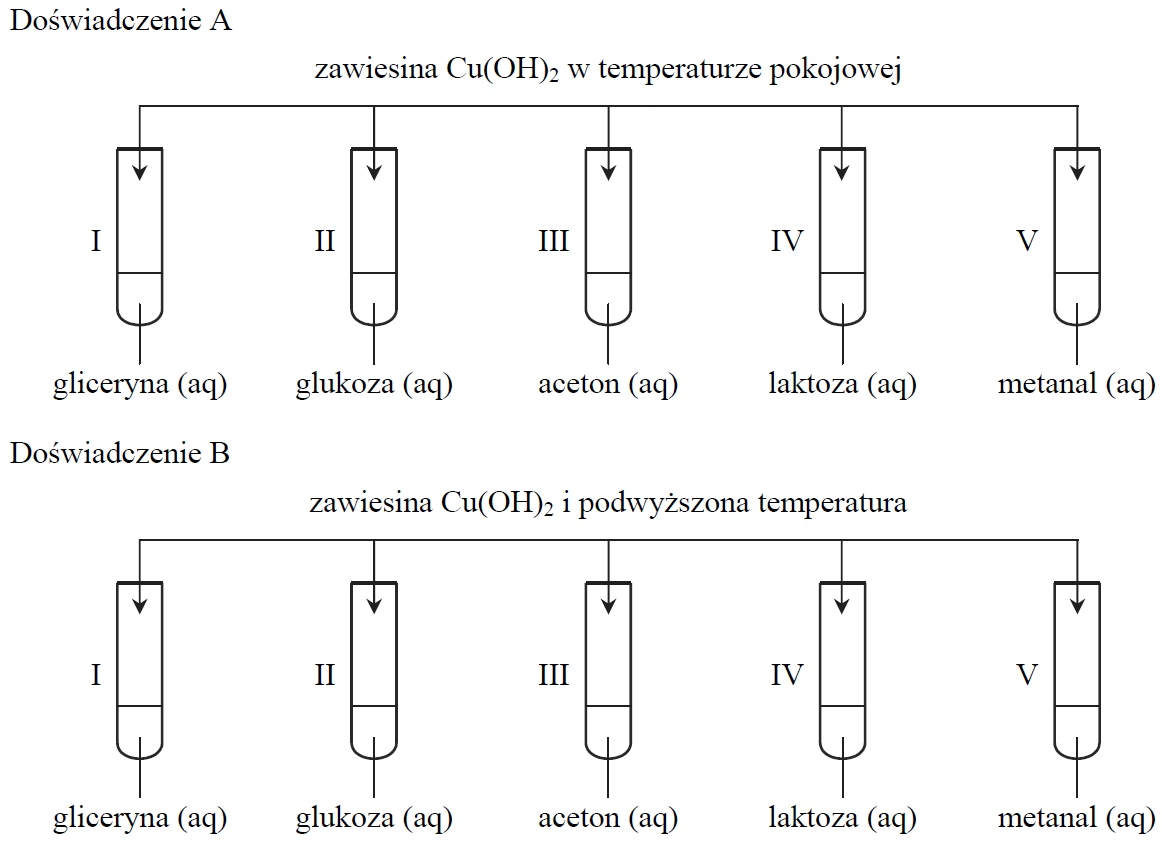
Reakcja glicerolu z wodorotlenkiem miedzi(II) ma praktyczne zastosowanie w chemii, szczególnie w identyfikacji polioli, czyli związków organicznych zawierających wiele grup hydroksylowych. Jest to tak zwana próba Trommera, choć w praktyce często stosuje się zmodyfikowane wersje tej próby. Pozytywny wynik próby (zmiana koloru na ciemnoniebieski i rozpuszczenie osadu) wskazuje na obecność polioli w badanej substancji.
Oprócz glicerolu, pozytywny wynik próby Trommera dają również inne poliole, takie jak:
- Cukry redukujące (np. glukoza, fruktoza, maltoza)
- Inne alkohole polihydroksylowe (np. mannitol, sorbitol)
Warto zaznaczyć, że reakcja ta jest charakterystyczna dla polioli i pozwala odróżnić je od innych grup związków organicznych, które nie dają pozytywnego wyniku w próbie Trommera.
Inne Reakcje Wodorotlenku Miedzi(II)
Wodorotlenek miedzi(II) reaguje nie tylko z glicerolem, ale także z innymi substancjami. Jedną z istotnych reakcji jest reakcja z roztworem amoniaku. Po dodaniu roztworu amoniaku do wodorotlenku miedzi(II), osad rozpuszcza się, tworząc klarowny, intensywnie szafirowy roztwór. Jest to spowodowane powstaniem jonu kompleksowego tetraaminomiedzi(II), o wzorze [Cu(NH3)4]2+.
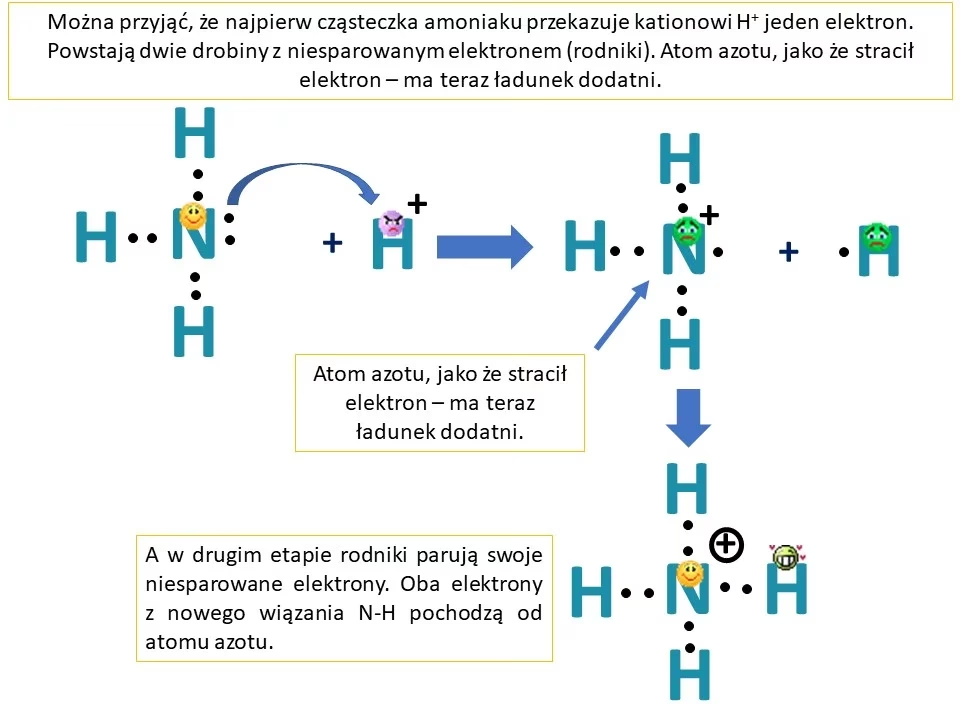
Reakcja z amoniakiem zachodzi w następujący sposób:
Cu(OH)2 (s) + 4NH3 (aq) ⇌ [Cu(NH3)4]2+ (aq) + 2OH- (aq)
Jon tetraaminomiedzi(II) jest kompleksem koordynacyjnym, w którym cztery cząsteczki amoniaku koordynują się wokół centralnego jonu miedzi(II). Podobnie jak w przypadku kompleksu z glicerolem, powstanie tego kompleksu jest związane z właściwościami jonu miedzi(II) do tworzenia wiązań koordynacyjnych.
Ponadto, wodorotlenek miedzi(II) w obecności tlenu może utleniać amoniak. W wyniku tej reakcji powstają azotyny miedzioaminowe. Przykładowym produktem takiej reakcji może być Cu(NO2)2(NH3)n, gdzie 'n' oznacza liczbę cząsteczek amoniaku w kompleksie. Ta reakcja jest bardziej złożona i zależy od warunków, w jakich przebiega, w tym od stężenia amoniaku i dostępu tlenu.
Podsumowanie Reakcji Wodorotlenku Miedzi(II)
Wodorotlenek miedzi(II) jest związkiem chemicznym o bogatej chemii reakcji. Reaguje on z glicerolem w środowisku zasadowym, tworząc charakterystyczny, ciemnoniebieski kompleks, co jest wykorzystywane do identyfikacji polioli. Ponadto, reaguje z roztworem amoniaku, tworząc jon tetraaminomiedzi(II) o szafirowej barwie, a także może utleniać amoniak w obecności tlenu do azotynów miedzioaminowych.
Te reakcje demonstrują zdolność jonu miedzi(II) do tworzenia kompleksów i uczestniczenia w reakcjach redoks. Zrozumienie tych reakcji jest istotne w chemii analitycznej, nieorganicznej i organicznej, a także w różnych zastosowaniach praktycznych, gdzie wykorzystuje się właściwości wodorotlenku miedzi(II).
Często Zadawane Pytania (FAQ)
- Czy wodorotlenek miedzi(II) jest rozpuszczalny w wodzie?
Wodorotlenek miedzi(II) jest słabo rozpuszczalny w wodzie. Jest to substancja stała, która tworzy osad w środowisku wodnym. Jednak w reakcji z glicerolem w środowisku zasadowym, kompleks miedzi(II) z glicerolem staje się rozpuszczalny, co objawia się rozpuszczeniem osadu i zmianą koloru roztworu. - Dlaczego reakcja glicerolu z wodorotlenkiem miedzi(II) daje niebieski kolor?
Niebieski kolor w reakcji glicerolu z wodorotlenkiem miedzi(II) jest spowodowany powstaniem kompleksu koordynacyjnego. Jony miedzi(II) w kompleksach często wykazują intensywne barwy, a w przypadku kompleksu z glicerolem jest to charakterystyczny ciemnoniebieski kolor. - Jakie inne związki oprócz glicerolu reagują z wodorotlenkiem miedzi(II) dając pozytywny wynik próby Trommera?
Oprócz glicerolu, pozytywny wynik próby Trommera dają inne poliole, szczególnie cukry redukujące, takie jak glukoza, fruktoza i maltoza, a także inne alkohole polihydroksylowe, np. mannitol i sorbitol. - Czy wodorotlenek miedzi(II) reaguje z kwasami?
Tak, wodorotlenek miedzi(II) jest zasadą i reaguje z kwasami, tworząc sole miedzi(II) i wodę. Na przykład, reakcja z kwasem solnym (HCl) prowadzi do powstania chlorku miedzi(II) i wody: Cu(OH)2 + 2HCl → CuCl2 + 2H2O. - Czy jon tetraaminomiedzi(II) jest trwały?
Jon tetraaminomiedzi(II) jest stosunkowo trwały w roztworze amoniakalnym. Jednak jego trwałość zależy od warunków, takich jak stężenie amoniaku i pH roztworu. W środowisku kwaśnym kompleks ulega rozkładowi, uwalniając jony miedzi(II) i amoniak.
Jeśli chcesz poznać inne artykuły podobne do Glicerol a Wodorotlenek Miedzi: Reakcja i Zastosowania, możesz odwiedzić kategorię HVAC.