28/05/2019
Nadmanganian potasu (KMnO4), znany również jako potasowy nadmanganian, jest silnym utleniaczem o charakterystycznym, intensywnym fioletowym kolorze. W laboratoriach chemicznych i nie tylko, często wykorzystuje się go w różnorodnych reakcjach, a także jako środek dezynfekujący. Jedną z interesujących właściwości KMnO4 jest jego zachowanie pod wpływem wysokiej temperatury. Co się dzieje, gdy podgrzejemy kryształy nadmanganianu potasu do temperatury 513K (240°C)? Proces ten, znany jako rozkład termiczny, prowadzi do powstania kilku interesujących produktów.

Podczas ogrzewania suchych kryształów KMnO4, które w temperaturze pokojowej mają niemal czarny kolor, zachodzi reakcja rozkładu. W efekcie obserwujemy powstanie czarnej pozostałości. Aby lepiej zrozumieć, co się wydarzyło, możemy przeprowadzić prosty eksperyment. Do czarnej pozostałości dodajemy niewielką ilość wody, a następnie całość filtrujemy. Okazuje się, że otrzymujemy zielony przesącz i czarny osad. Te obserwacje są kluczowe do zrozumienia reakcji, która zaszła.
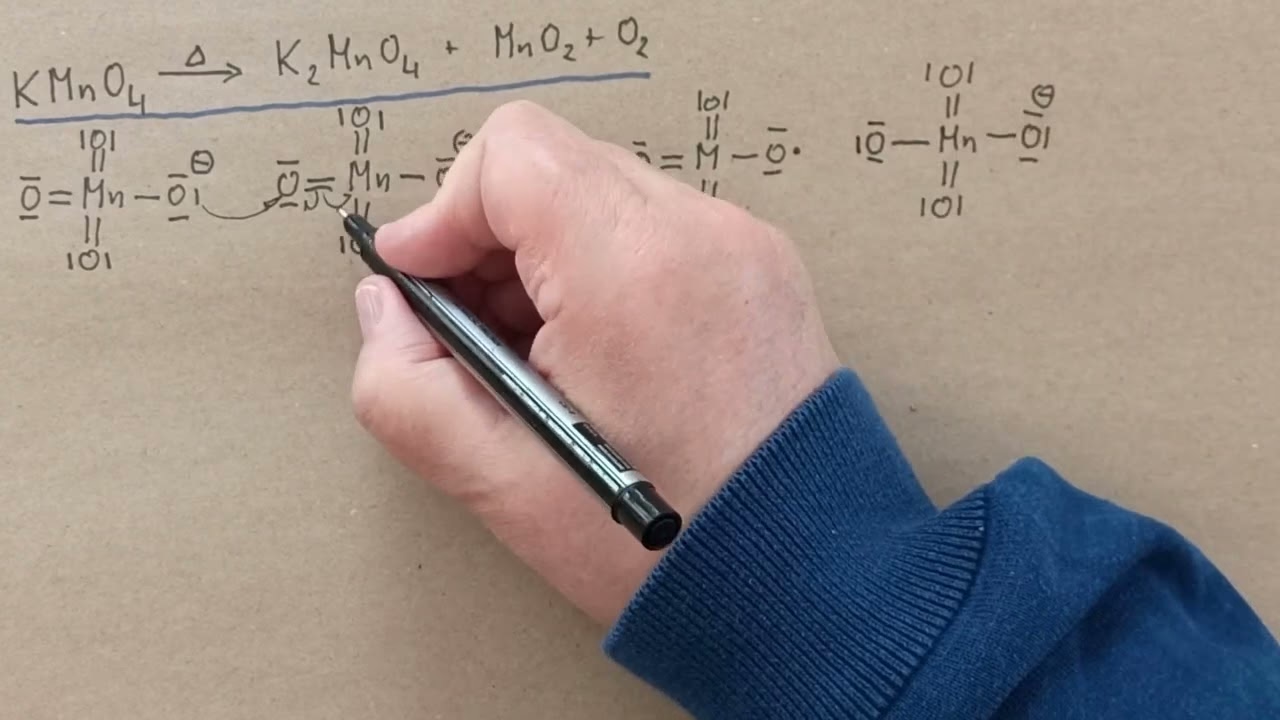
Reakcja rozkładu termicznego nadmanganianu potasu
Reakcję rozkładu termicznego nadmanganianu potasu można zapisać następującym równaniem chemicznym:
2KMnO4 → K2MnO4 + MnO2 + O2
Z równania tego wynika, że ogrzewanie nadmanganianu potasu (KMnO4) prowadzi do powstania trzech produktów: manganianu potasu (K2MnO4), tlenku manganu(IV) (MnO2) oraz tlenu (O2).
Charakterystyka produktów reakcji
- Manganian potasu (K2MnO4): Jest to związek o zielonym kolorze. Co ważne, manganian potasu jest dobrze rozpuszczalny w wodzie. To wyjaśnia, dlaczego po dodaniu wody do pozostałości po rozkładzie i filtracji, otrzymujemy zielony przesącz.
- Tlenek manganu(IV) (MnO2): Tlenek manganu(IV), znany również jako dwutlenek manganu, jest substancją stałą o czarnym kolorze i jest nierozpuszczalny w wodzie. To właśnie MnO2 stanowi czarny osad, który pozostaje po filtracji.
- Tlen (O2): Tlen jest gazem, który uwalnia się podczas reakcji. Można go zidentyfikować, na przykład, poprzez wprowadzenie tlącego się łuczywa do probówki, w której zachodzi reakcja – w obecności tlenu łuczywo powinno się rozpalić.
Analiza stopnia utlenienia manganu
Reakcja rozkładu termicznego nadmanganianu potasu jest przykładem reakcji redoks, a konkretnie dysproporcjonowania. W nadmanganianie potasu stopień utlenienia manganu wynosi +7. W manganianie potasu stopień utlenienia manganu obniża się do +6, natomiast w tlenku manganu(IV) stopień utlenienia manganu wynosi +4. Zatem, mangan ulega zarówno redukcji (obniżenie stopnia utlenienia do +6 i +4), jak i utlenieniu (w kontekście powstawania tlenu, choć sam mangan się nie utlenia w tym sensie, reakcja jako całość jest redoks).
Reakcje dysproporcjonowania charakteryzują się tym, że ten sam pierwiastek w określonym stopniu utlenienia ulega jednocześnie utlenieniu i redukcji.
Dalsze reakcje tlenku manganu(IV) (MnO2)
Chociaż głównym tematem jest rozkład termiczny KMnO4, warto wspomnieć o dalszych reakcjach tlenku manganu(IV) (MnO2), który jest jednym z produktów rozkładu. MnO2, reagując z chlorkiem sodu (NaCl) i stężonym kwasem siarkowym (H2SO4), może dać ostry w zapachu gaz – chlor (Cl2). Reakcja ta przebiega według równania:
MnO2 + 2NaCl + 2H2SO4 → MnSO4 + Cl2 + Na2SO4 + 2H2O
Ta reakcja jest wykorzystywana jako test na obecność anionów chlorkowych. Działanie stężonym kwasem siarkowym i tlenkiem manganu(IV) na stały chlorek prowadzi do wydzielenia żółtozielonego gazu o charakterystycznym, duszącym zapachu chloru.
Podsumowanie
Ogrzewanie nadmanganianu potasu (KMnO4) do temperatury 513K (240°C) powoduje jego rozkład termiczny. Produktami tej reakcji są manganian potasu (K2MnO4), tlenek manganu(IV) (MnO2) oraz tlen (O2). Manganian potasu jest zielony i rozpuszczalny w wodzie, tlenek manganu(IV) jest czarny i nierozpuszczalny w wodzie, a tlen jest gazem. Reakcja ta jest przykładem reakcji dysproporcjonowania, w której mangan zmienia swój stopień utlenienia z +7 w KMnO4 na +6 w K2MnO4 i +4 w MnO2. Rozkład termiczny KMnO4 jest klasyczną reakcją chemiczną, często demonstrowaną w laboratoriach i edukacji chemicznej, ilustrującą właściwości związków manganu i reakcje redoks.
Najczęściej zadawane pytania (FAQ)
- Jaki jest kolor nadmanganianu potasu (KMnO4)?
Nadmanganian potasu ma intensywny fioletowy, niemal czarny kolor w postaci kryształów. - Co się dzieje z kolorem podczas rozkładu termicznego KMnO4?
Fioletowy kolor KMnO4 zanika. Powstaje zielony manganian potasu (K2MnO4) i czarny tlenek manganu(IV) (MnO2). - Czy manganian potasu (K2MnO4) jest rozpuszczalny w wodzie?
Tak, manganian potasu jest dobrze rozpuszczalny w wodzie, co objawia się zielonym przesączem po dodaniu wody do pozostałości po reakcji. - Czy tlenek manganu(IV) (MnO2) jest rozpuszczalny w wodzie?
Nie, tlenek manganu(IV) jest praktycznie nierozpuszczalny w wodzie, tworząc czarny osad. - Jaki gaz powstaje podczas rozkładu termicznego KMnO4?
Podczas rozkładu termicznego nadmanganianu potasu powstaje tlen (O2). - Czy reakcja rozkładu termicznego KMnO4 jest reakcją redoks?
Tak, jest to reakcja redoks, a konkretnie reakcja dysproporcjonowania, gdzie mangan ulega zarówno redukcji, jak i (w kontekście reakcji jako całości) utlenieniu.
Jeśli chcesz poznać inne artykuły podobne do Rozkład termiczny KMnO4: Co powstaje podczas ogrzewania?, możesz odwiedzić kategorię HVAC.
