13/01/2018
Reakcja chemiczna to proces, w wyniku którego substancje zwane substratami przekształcają się w nowe substancje o odmiennych właściwościach, zwane produktami. Nie chodzi tu jedynie o zmianę stanu skupienia, ale o fundamentalną przemianę na poziomie molekularnym. Reakcje chemiczne są wszechobecne i odgrywają kluczową rolę w naszym życiu i otaczającym nas świecie.
https://www.youtube.com/watch?v=0gcJCfcAhR29_xXO
Przykłady reakcji chemicznych w życiu codziennym
Zdumiewające jest, jak wiele reakcji chemicznych zachodzi wokół nas każdego dnia. Często nawet nie zdajemy sobie z tego sprawy, obserwując codzienne zjawiska:
- Spalanie gazu w kuchence – reakcja, która dostarcza nam ciepło do gotowania.
- Jełczenie masła – proces, w którym tłuszcze ulegają rozkładowi, zmieniając smak i zapach.
- Kwaśnienie mleka – przemiana laktozy w kwas mlekowy, nadająca mleku charakterystyczny kwaśny smak.
- Osadzanie się kamienia w czajniku – wytrącanie się soli mineralnych z wody pod wpływem temperatury.
- Rdzewienie żelaza – powolne utlenianie żelaza w obecności tlenu i wilgoci, prowadzące do powstania rdzy.
Rodzaje reakcji chemicznych
Reakcje chemiczne można klasyfikować na różne sposoby. Jednym z podstawowych podziałów jest rozróżnienie na:
Reakcja syntezy (łączenia)
Reakcja syntezy, zwana również reakcją łączenia, zachodzi, gdy co najmniej dwie substancje (pierwiastki lub związki chemiczne) łączą się, tworząc jedną, nową substancję. Produkt reakcji syntezy ma zupełnie inne właściwości niż substraty. Szczególnym przypadkiem reakcji syntezy jest reakcja utleniania.
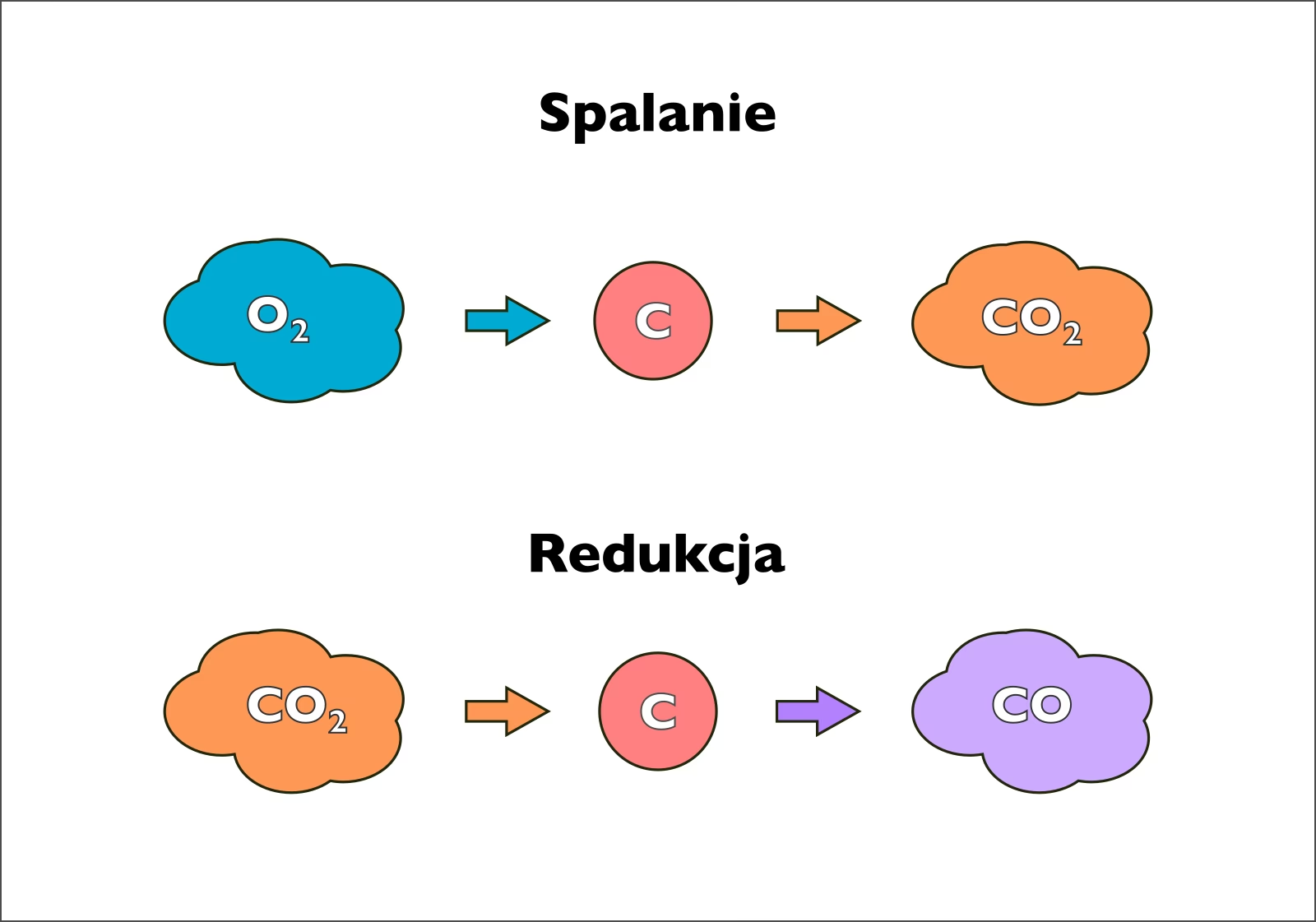
Reakcja utleniania
Reakcja utleniania polega na łączeniu się substancji z tlenem. W wyniku utleniania powstają tlenki – związki chemiczne, w których tlen łączy się z innym pierwiastkiem. Na przykład, rdzewienie żelaza jest powolną reakcją utleniania żelaza z tlenem zawartym w powietrzu, prowadzącą do powstania tlenku żelaza (rdzy). Gdy reakcja utleniania przebiega gwałtownie, z wydzielaniem ciepła i światła, mówimy o spalaniu. Klasycznym przykładem spalania jest reakcja magnezu z tlenem, która przebiega z intensywnym błyskiem i wydzielaniem dużej ilości energii.
Reakcja analizy (rozkładu)
Reakcja analizy, inaczej reakcja rozkładu, to proces odwrotny do syntezy. W reakcji analizy jedna substancja ulega rozkładowi na co najmniej dwie różne, prostsze substancje. Przykładem reakcji analizy jest rozkład tlenku rtęci, który pod wpływem ogrzewania rozkłada się na rtęć i tlen. Innym przykładem jest elektroliza wody, gdzie woda pod wpływem prądu elektrycznego rozkłada się na wodór i tlen.

Reakcja wymiany
Reakcja wymiany zachodzi, gdy dwa reagenty wymieniają się swoimi składnikami, tworząc dwa nowe produkty. Możemy wyróżnić dwa główne typy reakcji wymiany: pojedynczą i podwójną.
Reakcja wymiany pojedynczej
W reakcji wymiany pojedynczej jeden pierwiastek wypiera inny pierwiastek z związku chemicznego. Na przykład, wrzucenie kawałka cynku do roztworu siarczanu miedzi(II) spowoduje, że cynk wyprze miedź, tworząc siarczan cynku i wydzielając miedź metaliczną.
Reakcja wymiany podwójnej
W reakcji wymiany podwójnej dwa związki chemiczne wymieniają się jonami. Zwykle reakcja ta zachodzi w roztworach wodnych i prowadzi do powstania osadu, gazu lub słabo zdysocjowanego związku, np. wody. Przykładem reakcji wymiany podwójnej jest reakcja między roztworem azotanu srebra i roztworem chlorku sodu. W wyniku tej reakcji powstaje nierozpuszczalny chlorek srebra (osad) i azotan sodu.
Reakcje utleniania-redukcji (redoks)
Reakcje utleniania-redukcji, zwane również reakcjami redoks, to reakcje, w których następuje zmiana stopni utlenienia atomów. Reakcje utleniania i redukcji zawsze zachodzą jednocześnie. Utlenianie to proces oddawania elektronów przez atom, jon lub cząsteczkę, co powoduje wzrost stopnia utlenienia. Redukcja to proces przyjmowania elektronów, co prowadzi do obniżenia stopnia utlenienia. Wiele reakcji, które omówiliśmy wcześniej, np. spalanie i rdzewienie, to w rzeczywistości reakcje redoks.
Reakcje egzoenergetyczne i endoenergetyczne
Reakcje chemiczne można również klasyfikować ze względu na efekt energetyczny, jaki im towarzyszy. Wyróżniamy:
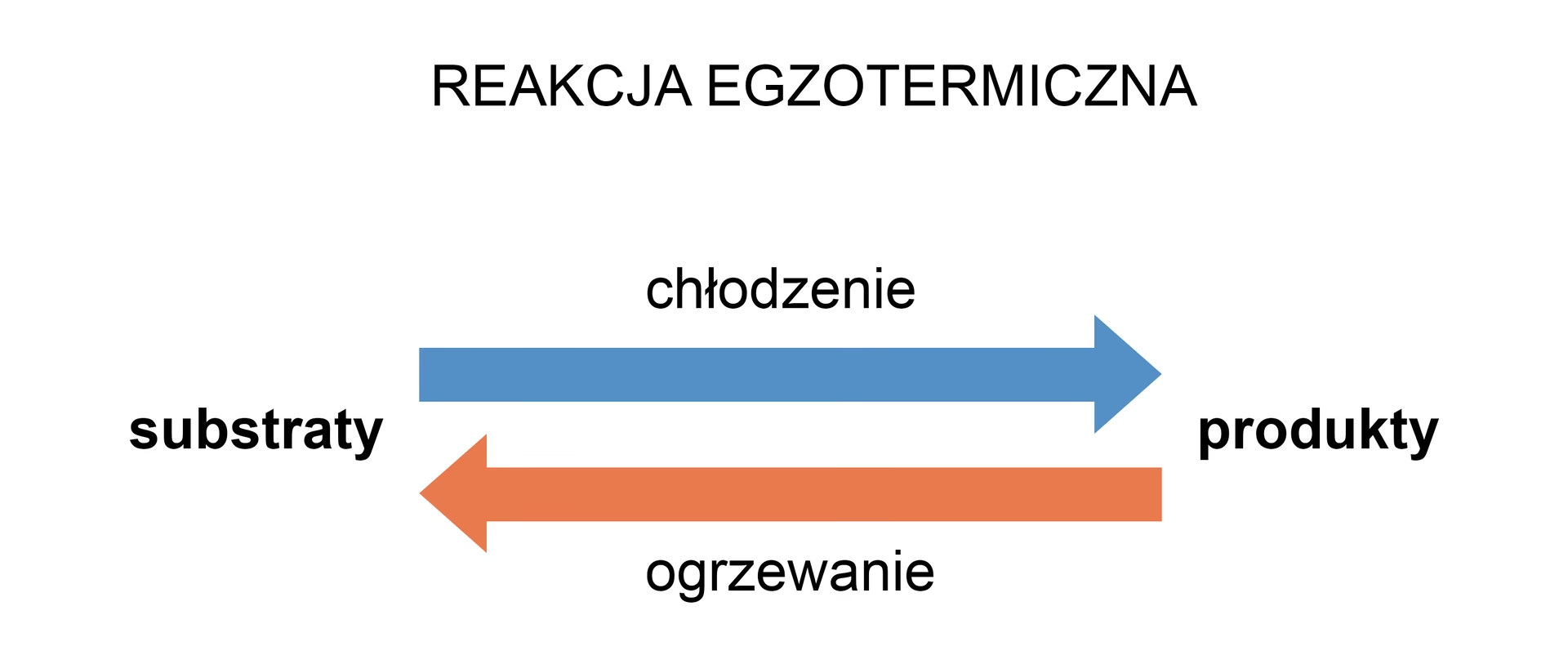
Reakcje egzoenergetyczne
Reakcje egzoenergetyczne to reakcje chemiczne, które wydzielają energię do otoczenia, najczęściej w postaci ciepła. Oznacza to, że produkty reakcji mają mniejszą energię niż substraty. Charakterystyczne dla reakcji egzoenergetycznych jest ujemna entalpia reakcji (ΔH < 0). Przykładem reakcji egzoenergetycznej jest reakcja tlenku wapnia z wodą (gaszenie wapna), która jest silnie egzotermiczna i wydziela dużo ciepła.
Reakcje endoenergetyczne
Reakcje endoenergetyczne to reakcje chemiczne, które pobierają energię z otoczenia, aby mogły zajść. Zazwyczaj energia ta jest dostarczana w postaci ciepła, ale może to być również energia świetlna lub elektryczna. Produkty reakcji endoenergetycznych mają większą energię niż substraty. Charakterystyczne dla tych reakcji jest dodatnia entalpia reakcji (ΔH > 0). Przykładem reakcji endoenergetycznej jest wspomniany wcześniej rozkład tlenku rtęci, który wymaga ciągłego ogrzewania, aby reakcja mogła przebiegać.

Jak rozpoznać, że zachodzi reakcja chemiczna?
Istnieje kilka wskazówek, które mogą sugerować, że zaszła reakcja chemiczna:
- Zmiana koloru – np. zmiana barwy roztworu lub pojawienie się osadu o innym kolorze.
- Wydzielanie się gazu – np. pojawienie się pęcherzyków gazu.
- Powstawanie osadu – wytrącanie się substancji nierozpuszczalnej z roztworu.
- Zmiana temperatury – wydzielanie ciepła (reakcja egzotermiczna) lub ochłodzenie (reakcja endotermiczna).
- Wydzielanie światła – np. płomień podczas spalania.
- Zmiana zapachu – powstanie nowego zapachu, innego niż zapach substratów.
Warto jednak pamiętać, że nie każda zmiana jest reakcją chemiczną. Na przykład, rozpuszczanie cukru w wodzie to zmiana fizyczna, a nie chemiczna, ponieważ cukier nie przekształca się w nową substancję.
Najczęściej zadawane pytania (FAQ)
- Co to jest reaktywność chemiczna?
- Reaktywność to zdolność substancji do wchodzenia w reakcje chemiczne. Substancje o wysokiej reaktywności łatwo reagują z innymi substancjami, natomiast substancje o niskiej reaktywności są mniej skłonne do reakcji. Przykładem substancji o niskiej reaktywności są metale szlachetne, takie jak złoto i platyna.
- Czym różnią się substraty od produktów?
- Substraty to substancje wyjściowe, które biorą udział w reakcji chemicznej. Produkty to substancje, które powstają w wyniku reakcji chemicznej.
- Czy wszystkie reakcje spalania są reakcjami utleniania?
- Tak, spalanie jest szczególnym przypadkiem reakcji utleniania, w którym reakcja przebiega gwałtownie, z wydzielaniem dużej ilości ciepła i światła.
- Czy reakcja endoenergetyczna może zachodzić samorzutnie?
- Zazwyczaj reakcje endoenergetyczne nie zachodzą samorzutnie i wymagają dostarczenia energii z zewnątrz. Jednak niektóre reakcje endoenergetyczne mogą zachodzić samorzutnie w specyficznych warunkach, np. przy odpowiednio wysokiej temperaturze, jeśli wzrost entropii układu jest wystarczająco duży, aby skompensować dodatnią entalpię.
Reakcje chemiczne są fundamentem chemii i otaczającego nas świata. Zrozumienie ich rodzajów i mechanizmów pozwala nam lepiej poznawać procesy zachodzące w przyrodzie i wykorzystywać je w praktyce, np. w przemyśle, medycynie i życiu codziennym.
Jeśli chcesz poznać inne artykuły podobne do Reakcje chemiczne: Przykłady i Rodzaje, możesz odwiedzić kategorię HVAC.