29/03/2026
Bezwodniki kwasowe stanowią interesującą grupę związków chemicznych o szerokim spektrum zastosowań. Charakteryzują się unikalnymi właściwościami, które wynikają z ich budowy molekularnej. W tym artykule przyjrzymy się bliżej bezwodnikom kwasowym, definiując je, omawiając metody ich syntezy oraz eksplorując ich różnorodne zastosowania.

Czym są bezwodniki? Definicja i podstawowe pojęcia
Słowo „bezwodnik” dosłownie oznacza „bez wody”. W chemii termin ten odnosi się do związków chemicznych powstałych w wyniku eliminacji wody z innej substancji. Bezwodniki reagują z wodą, tworząc z powrotem związek macierzysty, którym może być kwas lub zasada.

W kontekście kwasów, bezwodnik kwasowy definiuje się jako tlenek niemetalu, który w reakcji z wodą tworzy roztwór kwasowy. W chemii organicznej, bezwodnik kwasowy to grupa funkcyjna składająca się z dwóch grup acylowych połączonych atomem tlenu. Należy jednak pamiętać, że nie wszystkie tlenki niemetali są bezwodnikami kwasowymi; tylko te, które reagują z wodą, dając kwas, zasługują na to miano. Przykładem tlenku niemetalu, który nie jest bezwodnikiem kwasowym, jest tlenek węgla (monotlenek węgla, CO), ponieważ nie reaguje z wodą.
W chemii organicznej bezwodniki kwasowe powstają w wyniku dehydratacji dwóch grup kwasów karboksylowych.
Synteza bezwodników kwasowych
Bezwodniki kwasów organicznych można syntetyzować na różne sposoby. Jedną z metod jest ogrzewanie dwóch kwasów karboksylowych do wysokiej temperatury, rzędu 800°C. W tym procesie z reakcji usuwana jest cząsteczka wody. Innym sposobem jest reakcja kwasu karboksylowego z tlenkiem fosforu(V) (P2O5), który jest silnym środkiem odwadniającym.
Poniżej przedstawiono ogólny schemat syntezy bezwodnika kwasowego z dwóch kwasów karboksylowych:
[Schemat reakcji dehydratacji dwóch kwasów karboksylowych do bezwodnika kwasowego]
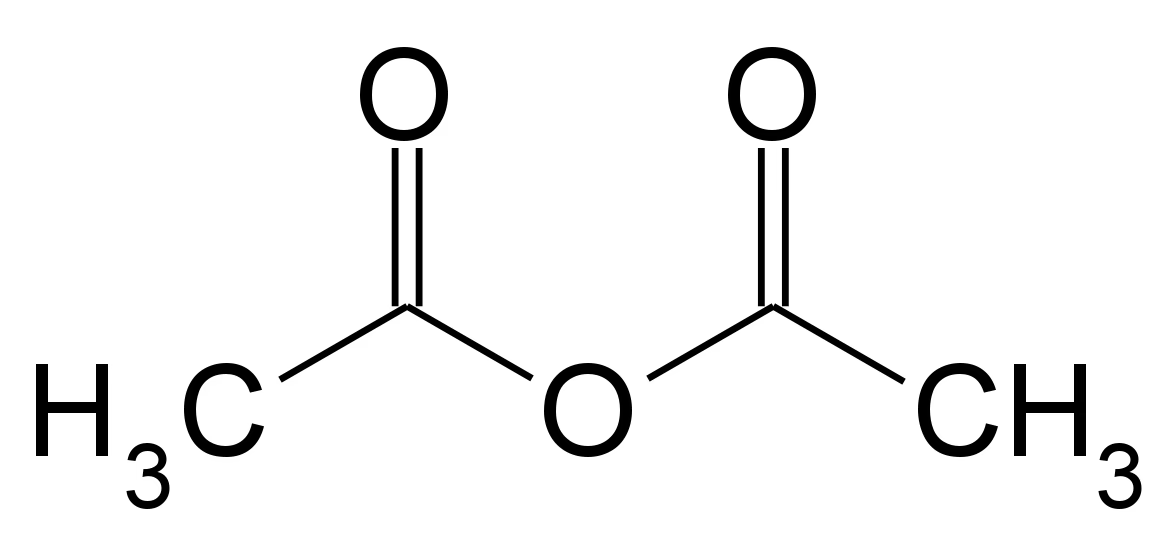
Bezwodniki kwasów karboksylowych zawierają dwie reszty kwasowe połączone mostkiem tlenowym (-O-). Mogą być symetryczne (pochodzące od dwóch identycznych kwasów) lub mieszane (pochodzące od dwóch różnych kwasów). Przykładem bezwodnika symetrycznego jest bezwodnik octowy, natomiast bezwodnikiem mieszanym jest bezwodnik mrówkowo-octowy.
Kwasy monokarboksylowe zazwyczaj nie tworzą bezwodników w wyniku prostej dehydratacji podczas ogrzewania. Wymagają zastosowania czynników kondensujących lub odwadniających, takich jak DCC (N,N'-dicykloheksylokarbodiimid) lub wspomniany tlenek fosforu(V). Reakcje kwasów lub ich soli z halogenkami kwasowymi również prowadzą do powstania bezwodników.
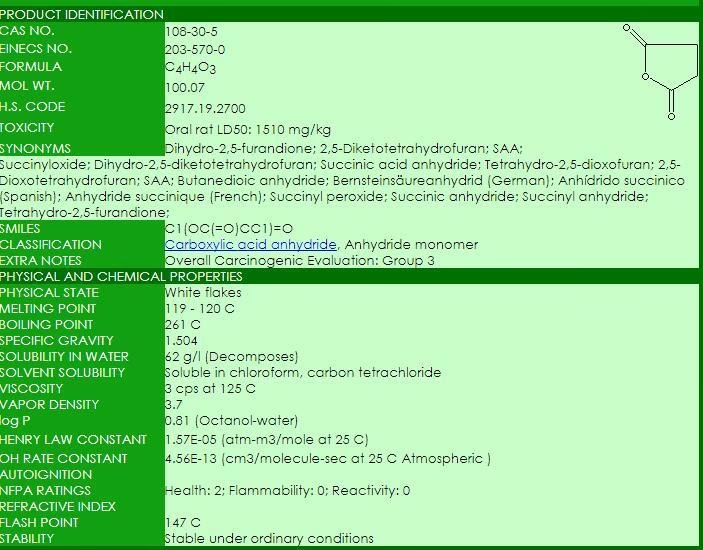
Bezwodniki zawierające grupę acetylową można otrzymać w reakcji kwasu z ketenem. Bezwodniki niektórych kwasów dikarboksylowych mogą powstawać w wyniku wewnątrzcząsteczkowego odszczepienia wody, często pod wpływem temperatury, prowadząc do cyklicznych bezwodników, takich jak bezwodnik ftalowy czy bezwodnik bursztynowy.
Właściwości chemiczne bezwodników kwasowych
Bezwodniki kwasowe charakteryzują się wysoką reaktywnością. Ulegają reakcjom nukleofilowego podstawienia, gdzie grupa -OCOR jest podstawiana przez nukleofil. Są mniej reaktywne niż chlorki kwasowe, ponieważ atom chloru jest bardziej elektroujemny niż grupa -OCOR.
Reakcje bezwodników kwasowych z wodą prowadzą do odtworzenia kwasów karboksylowych. Jest to reakcja hydrolizy, która przebiega łatwo, zwłaszcza w obecności katalizatorów kwasowych lub zasadowych.
Bezwodniki kwasowe reagują również z alkoholami i fenolami, tworząc estry i kwasy karboksylowe. Reakcja ta nazywana jest estryfikacją. Jest to ważna reakcja w syntezie organicznej, wykorzystywana do otrzymywania różnorodnych estrów.
Z amoniakiem i aminami bezwodniki kwasowe reagują, tworząc amidy. Jest to reakcja amidowania, również istotna w syntezie organicznej, szczególnie w chemii leków i materiałów.
Przykłady bezwodników kwasowych i ich reakcji z wodą
Dwutlenek węgla (CO2) jest bezwodnikiem kwasu węglowego. Reagując z wodą, tworzy kwas węglowy (H2CO3):
CO2(g) + H2O → H2CO3(aq)
Ta reakcja ma istotne znaczenie w kontekście środowiskowym, ponieważ jest odpowiedzialna za kwaśne deszcze i wpływa na pH wód powierzchniowych i oceanów. Wzrost stężenia CO2 w atmosferze prowadzi do zwiększenia ilości kwasu węglowego, co ma negatywny wpływ na środowisko.
Trójtlenek siarki (SO3) jest bezwodnikiem kwasu siarkowego. Reakcja z wodą prowadzi do powstania kwasu siarkowego (H2SO4):
SO3(g) + H2O → H2SO4(aq)
Podobnie jak w przypadku dwutlenku węgla, reakcja trójtlenku siarki z wodą również przyczynia się do powstawania kwaśnych deszczy, mających szkodliwy wpływ na środowisko.

Zastosowania bezwodników kwasowych
Bezwodniki kwasowe znajdują szerokie zastosowanie w chemii organicznej i przemyśle. Są wykorzystywane w produkcji wielu substancji, w tym:
- Farmaceutyków: np. aspiryny (kwas acetylosalicylowy), która powstaje w wyniku acetylacji kwasu salicylowego bezwodnikiem octowym.
- Chemikaliów przemysłowych: jako reagenty w różnorodnych syntezach organicznych.
- Materiałów wybuchowych: np. HMX, którego synteza wykorzystuje bezwodnik octowy.
- Perfum: w syntezie substancji zapachowych.
Bezwodniki kwasowe są również stosowane do:
- Acetylacji alkoholi w syntezie estrów.
- Deacetylacji morfiny w syntezie heroiny.
- Jako grupy ochronne w syntezie organicznej, chroniąc grupy hydroksylowe lub aminowe przed niepożądanymi reakcjami.
Jak zrobić bezwodnik octowy? Metody syntezy
Bezwodnik octowy, znany również jako tlenek acetylu, jest ważnym odczynnikiem w chemii organicznej. Istnieje kilka metod jego syntezy, w tym:
Synteza z chlorku acetylu i octanu sodu
Reakcja chlorku acetylu z octanem sodu jest jedną z metod otrzymywania bezwodnika octowego. Wymaga ona użycia chlorku acetylu (CH3COCl) i octanu sodu (CH3COONa). Chlorek acetylu jest substancją żrącą i należy zachować ostrożność podczas pracy z nim. Octan sodu powinien być bezwodny, co można osiągnąć przez suszenie.
Przebieg syntezy polega na powolnym dodawaniu chlorku acetylu do bezwodnego octanu sodu, a następnie destylacji powstałego produktu. Ważne jest, aby aparatura była sucha, aby uniknąć hydrolizy bezwodnika octowego.
Synteza z chlorku siarki (I) i octanu sodu oraz synteza z siarki w bromie i octanu sodu to kolejne metody, które opisano szczegółowo w dostarczonym materiale źródłowym. Metody te są bardziej skomplikowane i potencjalnie niebezpieczne, wymagają specjalistycznego sprzętu i ostrożności ze względu na używane odczynniki, takie jak chlorek siarki, brom i siarka.
Należy pamiętać, że synteza bezwodnika octowego, ze względu na jego potencjalne zastosowanie w nielegalnej produkcji substancji odurzających, powinna być przeprowadzana z zachowaniem wszelkich środków bezpieczeństwa i wyłącznie w celach naukowych lub przemysłowych, zgodnie z obowiązującymi przepisami.
Podsumowanie
Bezwodniki kwasowe stanowią kluczową grupę związków w chemii, charakteryzującą się wysoką reaktywnością i szerokim spektrum zastosowań. Odgrywają istotną rolę w syntezie organicznej, przemyśle farmaceutycznym, chemicznym i innych dziedzinach. Zrozumienie ich właściwości i metod syntezy jest kluczowe dla chemików i specjalistów z pokrewnych dziedzin.
Często zadawane pytania (FAQ)
- Czym różni się bezwodnik kwasowy od estru?
- Bezwodnik kwasowy powstaje przez usunięcie wody z kwasu (lub dwóch kwasów). Jest bardzo reaktywny, szczególnie jako środek acylujący. Ester powstaje w reakcji kwasu z alkoholem. Estry są generalnie mniej reaktywne niż bezwodniki i mają inne właściwości oraz zastosowania.
- Czy bezwodniki kwasowe są bezpieczne?
- Niektóre bezwodniki kwasowe, takie jak bezwodnik octowy, są żrące i drażniące. Należy z nimi pracować ostrożnie, stosując odpowiednie środki ochrony osobistej i pracując w dobrze wentylowanym pomieszczeniu.
- Jak przechowywać bezwodnik octowy?
- Bezwodnik octowy jest higroskopijny i reaguje z wodą, dlatego należy go przechowywać w szczelnie zamkniętych pojemnikach, w suchym miejscu, z dala od wilgoci.
Jeśli chcesz poznać inne artykuły podobne do Bezwodniki kwasowe: Definicja, synteza i zastosowania, możesz odwiedzić kategorię HVAC.