15/07/2019
Aldehydy to grupa związków organicznych o charakterystycznej strukturze, składającej się z atomu węgla połączonego podwójnym wiązaniem z atomem tlenu, pojedynczym wiązaniem z atomem wodoru i pojedynczym wiązaniem z inną grupą (R), która może być atomem węgla lub wodoru (w przypadku formaldehydu). Ta struktura nadaje aldehydom unikalne właściwości fizyczne i chemiczne, które znajdują szerokie zastosowanie w różnych dziedzinach, od przemysłu po perfumerię.

Czym są aldehydy? Struktura i wiązania
Centralny atom węgla w aldehydach jest zazwyczaj hybrydyzowany sp2, co wpływa na geometrię cząsteczki. Grupa aldehydowa (–CHO) jest umiarkowanie polarna ze względu na elektroujemność atomu tlenu. Długość wiązania C=O wynosi około 120–122 pikometrów.
Właściwości fizyczne i charakterystyka aldehydów
Właściwości aldehydów są zróżnicowane i zależą od reszty cząsteczki (grupy R). Mniejsze aldehydy, takie jak formaldehyd i acetaldehyd, są rozpuszczalne w wodzie. Lotne aldehydy charakteryzują się ostrym, przenikliwym zapachem. Identyfikacja aldehydów jest możliwa za pomocą metod spektroskopowych:
- Spektroskopia IR: Wykazują silne pasmo νCO w pobliżu 1700 cm−1.
- Spektroskopia 1H NMR: Atom wodoru grupy formylowej (–CHO) absorbuje w pobliżu δH 9.5 do 10 ppm, co jest charakterystyczne dla aldehydów. Sygnał ten wykazuje charakterystyczne sprzężenie z protonami na atomie węgla α.
- Spektroskopia 13C NMR: Sygnał atomu węgla karbonylowego (C=O) pojawia się w zakresie δC 190 do 205 ppm, choć jest on zazwyczaj słabszy.
Występowanie i zastosowania aldehydów
Aldehydy występują naturalnie w wielu miejscach. Ślady aldehydów można znaleźć w olejkach eterycznych, gdzie często przyczyniają się do ich przyjemnego zapachu. Przykłady to aldehyd cynamonowy (cynamon), cytral (cytronella) i wanilina (wanilia). Większość cukrów to pochodne aldehydów (aldozy), które występują głównie w postaci półacetali, formy maskującej aldehyd. Na przykład, w roztworze wodnym tylko niewielka frakcja glukozy występuje jako aldehyd.
Aldehydy mają szerokie zastosowanie w przemyśle i życiu codziennym. Przykłady ważnych aldehydów i ich zastosowań:
- Formaldehyd: Produkowany na największą skalę (około 6 milionów ton rocznie). Głównie wykorzystywany do produkcji żywic w połączeniu z mocznikiem, melaminą i fenolem (np. bakelit). Jest również prekursorem diizocyjanianu difenylometanu (MDI), stosowanego do produkcji poliuretanów.
- Butyraldehyd: Produkowany w ilości około 2,5 miliona ton rocznie. Główny prekursor 2-etyloheksanolu, który jest stosowany jako plastyfikator.
- Acetaldehyd: Dawniej dominujący produkt, obecnie produkcja spadła poniżej 1 miliona ton rocznie. Głównie stosowany jako prekursor kwasu octowego.
- Inne aldehydy: Wiele innych aldehydów znajduje zastosowanie komercyjne jako prekursory alkoholi okso, stosowanych w detergentach. Niektóre aldehydy, produkowane w mniejszych ilościach, są używane jako składniki aromatów i perfum, np. aldehyd cynamonowy, cytral i lilial.
Dialdehydy
Dialdehydy to związki organiczne zawierające dwie grupy aldehydowe. Krótkie alifatyczne dialdehydy są czasami nazywane od kwasów dwukarboksylowych, z których pochodzą. Przykładem jest butanodial, znany również jako aldehyd bursztynowy (pochodzący od kwasu bursztynowego).
Aldehydy w perfumerii
Aldehydy odgrywają kluczową rolę w przemyśle perfumeryjnym. Charakteryzują się intensywnymi, często ostrymi zapachami, które mogą imitować wonie naturalne, takie jak kwiatowe, owocowe i cytrusowe. Aldehydy nie tylko dodają zapachu, ale także pełnią funkcję wzmacniaczy i utrwalaczy kompozycji perfumeryjnych. Pomagają związać wszystkie składniki, nadając perfumom gładkości i trwałości. Wpływają również na rozwój zapachu na skórze.
Przykłady aldehydów stosowanych w perfumerii:
- Aldehyd C10: Zapach gorzkiej skórki pomarańczy.
- Aldehyd C11: Zapach kolendry.
- Aldehyd C12: Zapach fiołka i bzu.
- Aldehyd C9: Zapach róży.
Choć Chanel No. 5 jest najbardziej znanym przykładem perfum aldehydowych, aldehydy były używane w perfumerii już wcześniej. Uważa się, że po raz pierwszy zostały użyte w 1882 roku w perfumach Fougère Royale Paula Parqueta. Niemniej jednak, Chanel No. 5 (1921) zapoczątkowało erę nowoczesnych perfum aldehydowych.
Bezpieczeństwo i reaktywność aldehydów
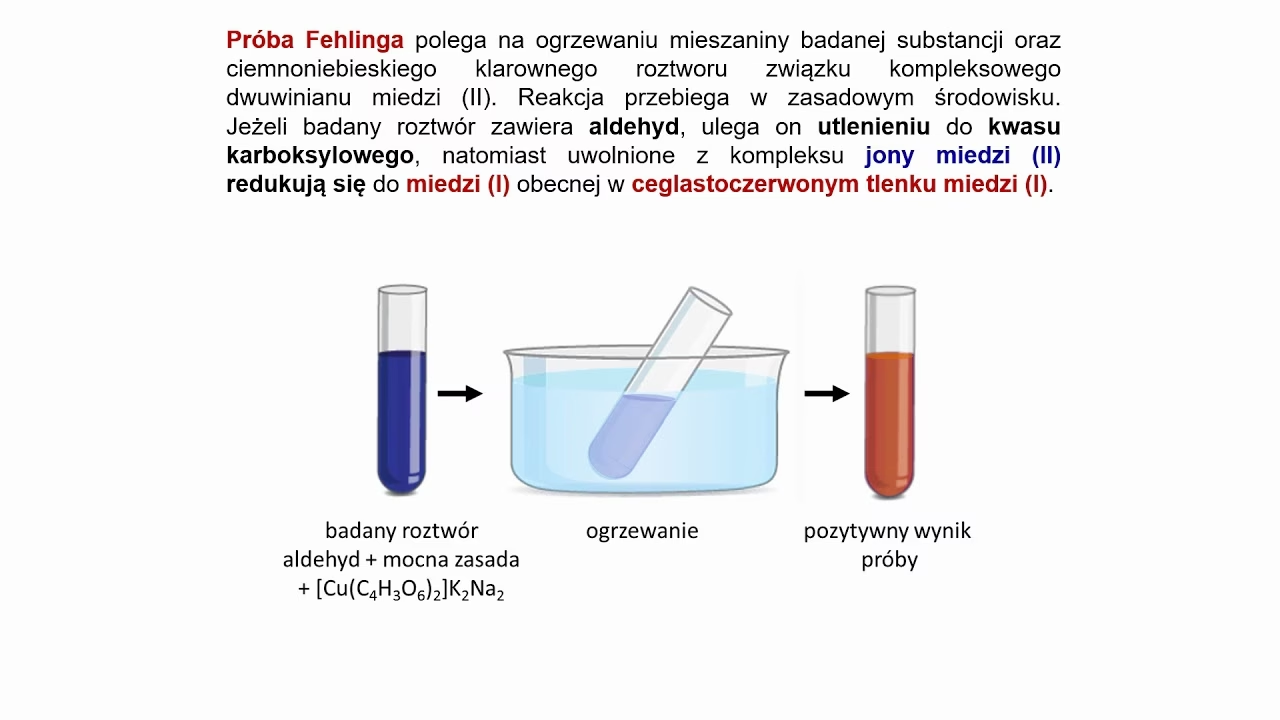
Aldehydy są reaktywne i mogą brać udział w różnych reakcjach chemicznych. Są łatwo utleniane do kwasów karboksylowych. Mogą również ulegać reakcjom samokondensacji i polimeryzacji, które są egzotermiczne i katalizowane przez kwasy i zasady.
Wiele aldehydów jest łatwopalnych, a mniejsze aldehydy, takie jak formaldehyd, acetaldehyd i akroleina, są szczególnie niebezpieczne ze względu na szerokie granice palności i niskie temperatury zapłonu (poniżej 38°C / 100°F). Autooksydacja aldehydów w powietrzu może prowadzić do powstania kwasów peroksy i ostatecznie kwasów karboksylowych. Reakcja ta jest aktywowana światłem, katalizowana przez sole metali przejściowych i autokatalityczna. Dodawanie stabilizatorów (antyoksydantów) do aldehydów opóźnia autooksydację. Rozproszenie aldehydów na materiałach o dużej powierzchni (np. ręczniki papierowe, szmaty) może przyspieszyć autooksydację i zwiększyć ryzyko pożaru.
Aldehydy mogą być toksyczne i działać drogą inhalacyjną, pokarmową i poprzez kontakt ze skórą. Niektóre aldehydy, takie jak akroleina i aldehyd krotonowy, są znane jako kancerogeny. Aldehydy mogą również działać jako sensybilizatory, wywołując reakcje alergiczne u niektórych osób. Formaldehyd i acetaldehyd, obecne w wielu produktach syntetycznych i spalinach, są dobrze udokumentowanymi alergenami.
Przykłady aldehydów
Przykłady aldehydów obejmują:
- Formaldehyd
- Acetaldehyd
- Propionaldehyd
- Butyraldehyd
- Walerianaldehyd
- Benzaldehyd
- Cynamaldehyd
- Akroleina
- Aldehyd krotonowy
Przykłady dialdehydów:
- Glioksal
- Malonaldehyd
- Aldehyd bursztynowy (Butanodial)
- Glutaraldehyd
Najczęściej zadawane pytania (FAQ)
- Co się dzieje, gdy aldehyd jest podgrzewany?
- Podgrzewanie aldehydów, zwłaszcza lotnych i łatwopalnych, zwiększa ryzyko pożaru ze względu na ich niską temperaturę zapłonu. Mogą również ulegać reakcjom utleniania i polimeryzacji pod wpływem ciepła. Należy zachować szczególną ostrożność podczas pracy z aldehydami w podwyższonej temperaturze.
- Jaki jest zapach aldehydowy?
- Zapach aldehydów jest zróżnicowany. Mniejsze aldehydy mają ostry, duszący zapach. W perfumerii stosuje się aldehydy o zapachach kwiatowych, owocowych i cytrusowych, które dodają kompozycjom świeżości i intensywności.
- Jakie są 3 główne zastosowania aldehydów?
- Trzy główne zastosowania aldehydów to: produkcja żywic (np. formaldehyd), produkcja plastyfikatorów (np. butyraldehyd) oraz jako składniki perfum i aromatów (różne aldehydy zapachowe).
- Jaka jest temperatura zapłonu aldehydów?
- Temperatura zapłonu aldehydów jest bardzo zróżnicowana i zależy od konkretnego aldehydu. Wiele aldehydów ma niskie temperatury zapłonu poniżej 38°C (100°F), co czyni je łatwopalnymi. Formaldehyd, acetaldehyd i akroleina są szczególnie niebezpieczne pod względem palności.
Aldehydy, mimo swojej reaktywności i potencjalnej toksyczności, są niezwykle ważnymi związkami chemicznymi o szerokim spektrum zastosowań. Zrozumienie ich właściwości i bezpieczne obchodzenie się z nimi jest kluczowe w wielu gałęziach przemysłu i nauki.
Jeśli chcesz poznać inne artykuły podobne do Aldehydy: Właściwości, zastosowania i bezpieczeństwo, możesz odwiedzić kategorię HVAC.
