25/03/2023
Octan sodu to związek chemiczny o niezwykłych właściwościach, które sprawiają, że jest on szeroko wykorzystywany w różnych dziedzinach, od przemysłu spożywczego po medycynę. Jednym z najbardziej intrygujących aspektów octanu sodu jest jego zachowanie pod wpływem temperatury. Co się zatem stanie, gdy podgrzejemy octan sodu?
Co to jest octan sodu?
Octan sodu, znany również jako etanian sodu, to sól sodowa kwasu octowego. Występuje w postaci białego, krystalicznego proszku o charakterystycznym, lekko octowym zapachu. Jest to substancja dobrze rozpuszczalna w wodzie i stosunkowo bezpieczna w użytkowaniu, co przyczynia się do jego popularności w wielu aplikacjach.

Podgrzewanie trójwodnego octanu sodu: eksperyment z krystalizacją
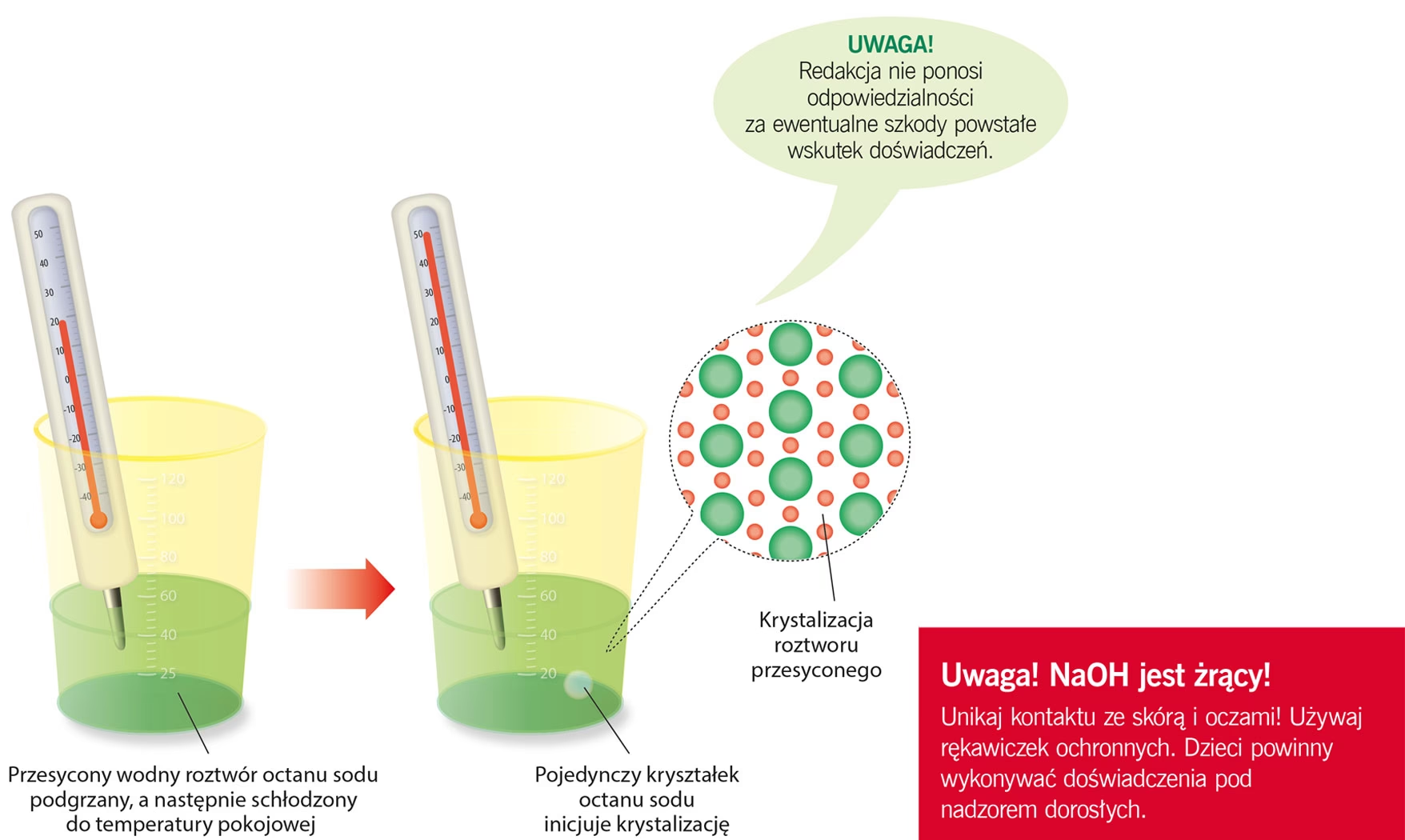
Jedną z najbardziej spektakularnych reakcji związanych z octanem sodu jest krystalizacja przesyconego roztworu. Aby to zademonstrować, możemy przeprowadzić prosty eksperyment:
- Rozpuść trójwodny octan sodu w minimalnej ilości wody, podgrzewając roztwór. Ważne jest, aby uzyskać roztwór nasycony, w którym nie pozostają żadne nierozpuszczone kryształki.
- Po całkowitym rozpuszczeniu substancji, ostrożnie ostudź roztwór do temperatury pokojowej, unikając wstrząsów i zanieczyszczeń. W ten sposób uzyskujemy roztwór przesycony – zawiera on więcej substancji rozpuszczonej, niż normalnie byłoby to możliwe w danej temperaturze.
- Dodaj do przesyconego roztworu niewielki kryształek octanu sodu.
Obserwacja będzie fascynująca! W momencie dodania kryształka, roztwór natychmiast zacznie krystalizować. Proces ten jest egzotermiczny, co oznacza, że wydziela ciepło. Roztwór stanie się gorący, a cała objętość w krótkim czasie zamieni się w stałą, krystaliczną masę przypominającą lód – stąd popularna nazwa „gorący lód”.
Wyjaśnienie tego zjawiska leży w naturze trójwodnego octanu sodu. Podczas podgrzewania powyżej 58°C, traci on wodę hydratacyjną i rozpuszcza się we własnej wodzie. Po ochłodzeniu, roztwór staje się przesycony w stosunku do trójwodnego octanu sodu. Dodanie kryształka „zasiewu” inicjuje krystalizację, podczas której octan sodu trójwodny wytrąca się z roztworu, uwalniając zgromadzoną energię w postaci ciepła.
Octan sodu i soda kaustyczna: reakcja dekarboksylacji
Podgrzewanie octanu sodu w obecności sody kaustycznej (mieszaniny wodorotlenku sodu i tlenku wapnia) prowadzi do innej ciekawej reakcji – dekarboksylacji. Jest to reakcja, w której z soli kwasu karboksylowego, w tym przypadku octanu sodu, powstaje alkan z mniejszą o jeden atom węgla liczbą atomów węgla niż kwas karboksylowy. Soda kaustyczna, czyli mieszanina wodorotlenku sodu (NaOH) i tlenku wapnia (CaO), odgrywa kluczową rolę w tej przemianie.
Reakcję dekarboksylacji octanu sodu z sodą kaustyczną można zapisać równaniem:
C{{H}_{3}}COONa + NaOH CaO, Δ → C{{H}_{4}} + Na{{H}_{2}}CO{{3}}
W wyniku tej reakcji, metan (CH4), najprostszy alkan, oraz węglan sodu (Na2CO3) jako produkt uboczny. Tlenek wapnia w sodzie kaustycznej pełni funkcję osuszającą i ułatwia manipulację wodorotlenkiem sodu, który jest higroskopijny.
Reakcja dekarboksylacji jest przydatna w chemii organicznej, szczególnie gdy chcemy skrócić łańcuch węglowy o jeden atom. Jeżeli chcielibyśmy otrzymać etan, należałoby użyć propionianu sodu zamiast octanu sodu.
Ogrzewacze do rąk i „gorący lód”
Praktyczne zastosowanie właściwości octanu sodu znajdziemy w popularnych ogrzewaczach do rąk wielokrotnego użytku. Wewnątrz takiego ogrzewacza znajduje się przesycony roztwór octanu sodu oraz metalowa płytka. Zgięcie płytki inicjuje krystalizację roztworu, co powoduje wydzielenie ciepła i ogrzanie ogrzewacza. Aby ogrzewacz był ponownie gotowy do użycia, wystarczy umieścić go w gorącej wodzie, aby rozpuścić kryształy octanu sodu i ponownie uzyskać roztwór przesycony.
Efekt „gorącego lodu” z octanu sodu jest również popularną demonstracją w laboratoriach chemicznych i na pokazach naukowych, ilustrującą w efektowny sposób proces krystalizacji i przemiany fazowe.
Inne eksperymenty z ciepłem: nie tylko octan sodu
Octan sodu to tylko jeden z przykładów substancji, które wykazują interesujące właściwości termiczne. Warto wspomnieć o innych doświadczeniach, które pozwalają zrozumieć naturę ciepła i energii:
- Mieszanie wody i alkoholu etylowego: Zmieszanie wody z alkoholem etylowym powoduje wzrost temperatury. Jest to spowodowane zmianami w wiązaniach wodorowych między cząsteczkami cieczy.
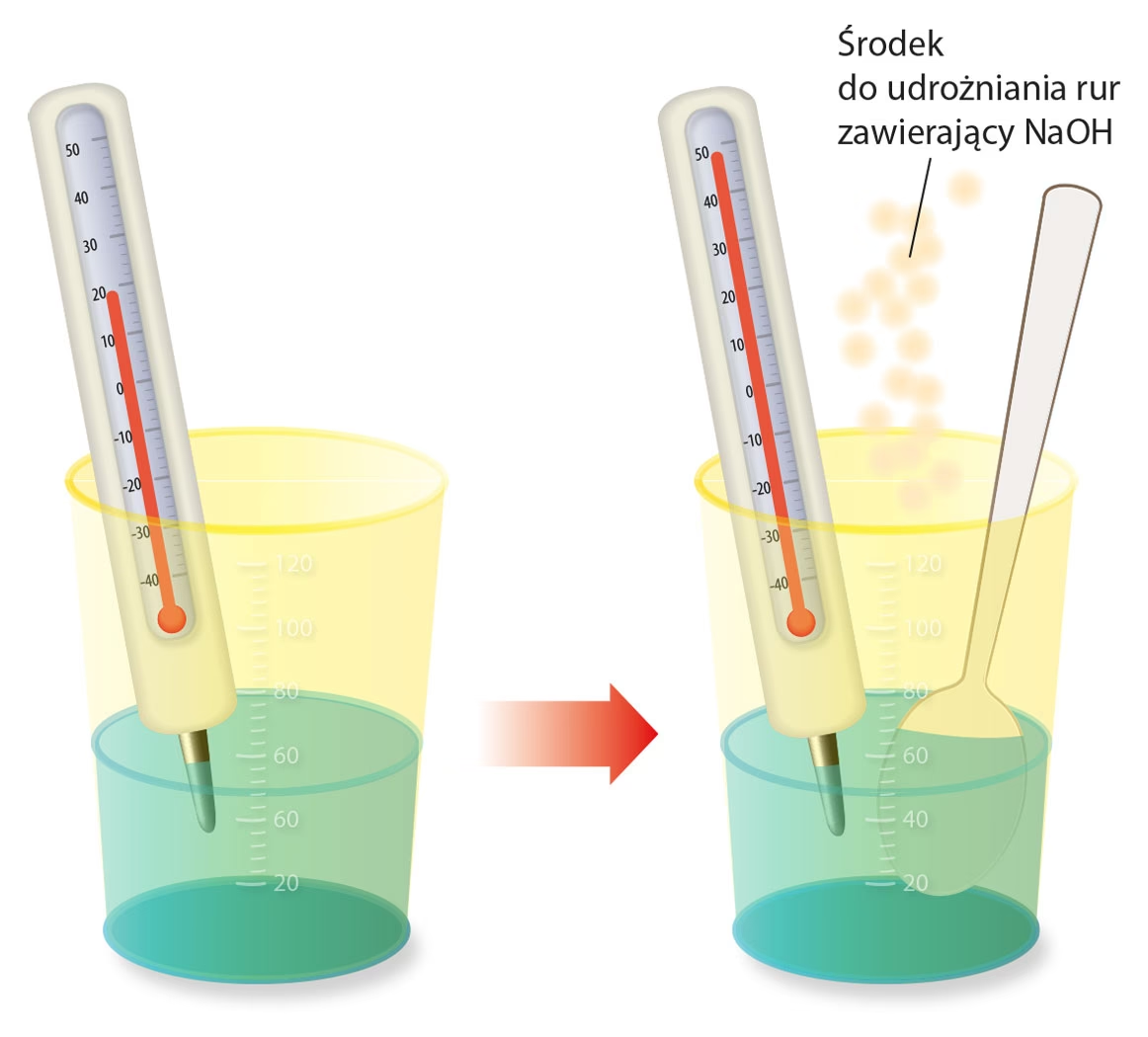
- Rozpuszczanie wodorotlenku sodu (NaOH) w wodzie: Jest to reakcja silnie egzotermiczna. Rozpuszczanie NaOH w wodzie powoduje znaczny wzrost temperatury roztworu.
Te przykłady ilustrują różnorodność zjawisk związanych z ciepłem i energią, które możemy obserwować i badać w chemii i fizyce.
Wiedza w pigułce: ciepło i energia w naszym świecie
Od zarania dziejów ludzkość wykorzystuje ciepło, początkowo z ognia, a obecnie z różnorodnych źródeł, od spalania paliw po zaawansowane technologie. Ciepło jest formą energii, która może być przekazywana na wiele sposobów. Kalorymetria pozwala na precyzyjne mierzenie zmian temperatury i ciepła w różnych procesach, od reakcji chemicznych po przemiany fazowe.

Zrozumienie procesów egzotermicznych i endotermicznych jest kluczowe w wielu dziedzinach, od projektowania reaktorów chemicznych po systemy ogrzewania i chłodzenia. Nawet pozornie proste zjawiska, jak krzepnięcie wody, wiążą się z wydzielaniem ciepła. Wykorzystanie tych zasad pozwala na tworzenie innowacyjnych technologii, takich jak pompy ciepła, które efektywnie ogrzewają pomieszczenia, wykorzystując nawet niskotemperaturowe źródła ciepła.
Podsumowanie
Podgrzewanie octanu sodu ujawnia fascynujące aspekty jego chemii. Od spektakularnej krystalizacji „gorącego lodu” po reakcję dekarboksylacji z sodą kaustyczną, octan sodu jest związkiem o bogatym spektrum właściwości termicznych. Jego praktyczne zastosowania, takie jak ogrzewacze do rąk, oraz demonstracje naukowe czynią go interesującym obiektem badań i edukacji, pozwalającym lepiej zrozumieć świat ciepła i energii wokół nas.
Jeśli chcesz poznać inne artykuły podobne do Octan sodu: fascynująca chemia ciepła i zimna, możesz odwiedzić kategorię HVAC.